Éhezés
Az éhezés… az emberek megfelelő táplálék nélkül mennek el, míg az éhínség az éhezés különösen virulens megnyilvánulása, amely széles körű halált okoz.
Kapcsolódó kifejezések:
- Aminosav
- Szőlőcukor
- Enzim
- Fehérje
- Inzulin
- Mutáció
- Autofágia
- Autophagosoma
Letöltés PDF formátumban
Erről az oldalról
Éhezés
Absztrakt
A halálos éhezés ritka halálozási ok az iparosodott országokban, de súlyos gyógyszerjogi jelentőségű lehet, ha a halál az élelmiszerek, különösen a csecsemők szándékos visszatartása miatt következik be. Az éhezés jelentősége klinikai, törvényszéki és medicolegal értelemben az alultápláltság mértékétől vagy az indukált metabolikus rendellenességektől függ, amelyek viszont függenek az éhezés súlyosságától és időtartamától, valamint attól, hogy összefüggenek-e súlyosbító tényezőkkel, például betegségekkel. Normális esetben az éhezés következtében bekövetkezett halál diagnosztizálása egyszerű prima facie diagnózis. Az alapbetegségeket, mint a soványodás okait, és az egyidejű betegségeket azonban ki kell zárni. A következő fejezetben az éhezés jelentőségére, a normál táplálkozási szükségletekre, a betegséggel összefüggő alultápláltságra, az éhezés mértékére, a boncolási eredményekre és a további vizsgálatokra kerül sor, amelyek fontosak egy gyógyszeres törvényi környezetben. A gyermekek éhezése esetén a fehérje-energia alultápláltság számos osztályozása különös jelentőséggel bír, amelyeket a harmadik világ országai számára fejlesztettek ki.
Éhezés
Absztrakt
Az éhezés olyan folyamat, amely az étkezés megemésztése után kezdődik, és addig tart, amíg az ételt ismét el nem fogyasztják; a kifejezést gyakran felváltva használják az éhezéssel, ami az étel bevitelének önkéntes megszüntetését jelenti. Jelentősebb anyagcsere-adaptációk fordulnak elő az éhezés kezelésére, amelyek közül a legjelentősebb az üzemanyag-váltás. Minden emlősnek, az embernek is, viszonylag kevés a szénhidráttartalma; egy 70 kg-os férfinak körülbelül 900 kcal szénhidrát van glikogénként tárolva a vázizomban és a májban, de a zsírszövetben 141 000 kcal triglicerid van. Az agy és a vörösvértestek üzemanyagként a glükózt használják (az agy hozzávetőlegesen 600 kcal d −1). Az éhezés során szintetizálódó glükóz (glükoneogenezis) aminosavakat használ szénforrásként. Az éhezés során bekövetkező sovány testtömeg-veszteség minimalizálása érdekében jelentős adaptációra van szükség ahhoz, hogy a zsírsavak és ezek oxidatív terméke, a ketontestek felhasználhatók legyenek az üzemanyag fő forrásai. Ez a cikk részletesen ismerteti az éhezés során bekövetkező anyagcsere-adaptációkat és a változások értékelésére alkalmazott módszereket.
Éhezés
Martin Kohlmeier, a tápanyagcserében, 2003
Fehérje forgalom
Míg az éhezés során jelentős mennyiségű testzsír veszhet el, a fő veszélyt a fehérje lebomlása okozza. A nyilvánvaló általános izomsorvadás baljóslatú jellemző, amely a funkcionális fehérjék párhuzamos veszteségére utal a szívben, a májban, a vesében és más szövetekben.
Körülbelül 150 g esszenciális aminosav és hasonló mennyiségű nem esszenciális aminosav szükséges naponta a fehérjék szintéziséhez egészséges, átlagos testsúlyú férfiban (Munro, 1975). Ennek nagy része a testfehérjék lebontásából származhat.
Amikor az energiafogyasztás megszűnik megfelelőnek lenni egy korábban jól táplált embernél, és az egynapos glikogénellátás elfogy, a sejtes szabad aminosavak, a rendszeres fehérjeforgalom és a kis fehérjetartalom fokozott mozgósítása különösen gyors forgalom mellett (" labilis fehérje ') fedezheti a böjt első óráinak glükózszükségletét. Főként az agy erős támaszkodása a folyamatos glükózellátáshoz teszi oly fontossá az aminosavakból származó glükoneogenezist.
A glükagon növekvő szekréciója a csökkenő vércukorszintre reagálva elősegíti a fehérje mobilizálódását a vázizomzatban és más szövetekben. A hidrolizált fehérje nagy része alaninként és glutaminként jut a vérbe. A máj és a vesék ezeket a nem esszenciális aminosavakat felhasználhatják a glükonkogenezishez, és a glükózt ismét kikerülhetik a keringésbe az agy, az izmok és más glükózfüggő szövetek felhasználására. A máj a glutamint is kiválasztja a vérbe, mint nitrogén és üzemanyag hordozó más szövetek számára (Watford et al., 2002). Az alaninciklus kifejezés utal az alanin használatára transzferként az izom és a máj közötti nitrogén- és szénátadásra. A szöveti fehérje megnövekedett lebomlása és a felszabadult aminosavak oxidációja nyilvánvaló a karbamidtermelés megkétszereződéséből az éhezés első napjaiban (Giesecke et al., 1989). A traumás stressz és fertőzés után a keringésben megnövekedő hormonok (adrenalin, kortizol) és citokinek (pl. Interleukin 6) gyorsan az intracelluláris szabad aminosavakra támaszkodnak (Hammarqvist et al., 2001), és felgyorsítják a fehérje katabolizmust (Smeets et al., 1995).
Ha az éhezés folytatódik, a test zsírraktár-szükséglete az energia egyre nagyobb hányadát képes kielégíteni. Még az agy is egyre jobban alkalmazkodik az acetoacetát és a β-hidroxi-butirát zsírsav-metabolitjaihoz. Javasolták azonban, hogy szöveti fehérjét kell mozgósítani a Krebs-ciklus közbenső termékeinek, az a-ketoglutarátnak és az oxaloacetátnak a feltöltésére (Owen és mtsai, 1998). Az emberi agy szokatlanul nagy glükózigénye, amely a gyermek teljes energiafelhasználásának akár a felét is kitöltheti, állandó lefolyást okoz a Krebs-ciklus közbenső termékeiben. A mobilizált trigliceridekből származó glicerin kielégítheti más kisagyú emlősök glükózszintézisének szükségességét, de emberben ez nem elég. Ennek ellenére az elhízott emberek éhezés során csak feleannyira veszítik el a szövetfehérjét, mint a sovány emberek (Elia et al., 1999). A zsírból származó glicerin hozzáférhetősége változhat.
A tartós éhezés megváltoztatja a fehérje- és aminosavcsere kulcsfontosságú enzimjeinek aktivitását (Young és Marchini, 1990). Összességében csökken a visszafordíthatatlan lebontásban részt vevő enzimek aktivitása, és az aminosavak újrafeldolgozásához és felhasználásához szükséges enzimek növekedése.
Az éhezés eredményeként az aminosavak oxidációja a fehérje forgalmából 10% alá csökken (Tomkins et al., 1983). Az aminosav-dehidrogenázok aktivitása az izmokban, valamint a karbamid ciklusa a májban és a vesékben csökken. Étrendi bevitel hiányában a portális vérből származó ammóniafelvétel nagymértékben meghaladja az aszpartátfelvételt. Ennek következménye, hogy a májfehérjéket mobilizálni kell az aszpartát előállításához az ammónia karbamid-méregtelenítéséhez (Brosnan et al., 2001).
2. kötet
Éhezési ketózis
Az éhezés szerény ketoacidózist eredményez normális egyénekben. Az első 10–14 órás éhezés során a glükózszintet elsősorban glikogenolízissel tartják fenn. A glikogénkészletek kimerülése után a glükoneogenezis válik a fő glükózforrássá. A máj energiaigényét a zsírsavak oxidációja tartja fenn. A felgyorsult lipolízis és a máj zsírsav oxidációja ketoacidózishoz vezet, amint azt korábban tárgyaltuk. 1-2 hét elteltével a vér ketoavkoncentrációja körülbelül 5-6 mEq/liter-re stabilizálódik, és a [HCO 3 -] p 18–20 mEq/literre csökken. A fulminánsabb ketoacidózis megszakad a ketoacid által kiváltott inzulin hasnyálmirigy-szigeti sejtekből történő felszabadulása következtében. 237 A folyamatos éhezés ellenére az ebből adódó inzulinszint növekedése tompítja a lipolízist. Folyamatos éhezés esetén a glükagon és a katekolamin szintje is a normális tartomány felé csökken, és ez szintén lelassítja a ketoavképződést. A terhes nők és a kisgyermekek azonban különösen ki vannak téve az éhezés során jelentkező súlyosabb ketoacidózisnak. Ilyen betegeknél az anorexia, a hányás és a hasi fájdalom miatt az orális táplálás gyakran lehetetlen.
Metabolikus homeosztázis
Fehérje katabolizmus éhezés során
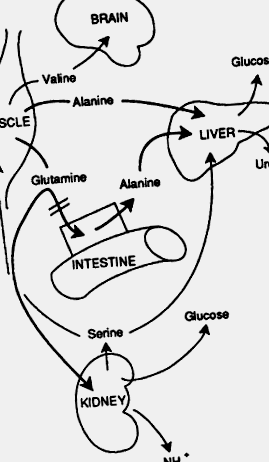
22-24. ÁBRA. Az aminosavak posztabszorpciós metabolizmusa és a sav-bázis metabolikus kapcsoló. A korai posztabszorpciós fázisban a máj az alaninból képződött plazma glükóz elsődleges forrása, amelyet izom vagy bél szállít. Az elsődleges nitrogéntermék a karbamid. Az éhezés előrehaladtával a sav-bázis egyensúly iránti igény csökkent glutaminfelvételt eredményez a splanchnic ágyban, és fokozza a vese felvételét. A vesében a glutamin ammónium-iont termel ellenionként a β-hidroxi-butirát és az acetoacetát számára. A glutamin szénláncát használják a glükoneogenezisben. Ha az éhezés előrehalad, a sav-bázis egyensúly iránti igény csökkent glutaminfelvételt eredményez a splanchnic ágyban, és fokozza a vese felvételét. Az elágazó láncú aminosavak az izom anyagcseréjének fő szubsztrátjai. Később az éhezés során az elágazó láncú aminosavak egy része, nevezetesen a valin, felszabadul az izmokból, és az agy energiaforrásként felhasználhatja őket.
22-25. ÁBRA. Az éhezés során a glükóztermelés forrásai.
[Sokszorosítva F. J. Cahill engedélyével, Az inzulin élettana az emberben: Diabetes 20, 783 (1971).]
Nem emlős hormon-viselkedési rendszerek
2.31.3.1 Éhezési stressz
Az éhezés ökológiailag releváns stresszor, mivel az élelmiszerek rendelkezésre állása a legtöbb környezet dinamikus aspektusa. Ezért azt feltételezhetjük, hogy az étkezéshiány kísérő viselkedési és fiziológiai reakciói jelentős szelektív nyomás alá kerültek, és hogy az éhezési válaszok hátterében álló mechanizmusok sokféle organizmusban hasonlóak lehetnek. A rovarokban az éhezési válaszok meghatározására a leggyakrabban használt mutató az élettartam, és lényegében két tényező határozza meg, hogy egy szervezet mennyi ideig élheti túl az éhezési kihívást. Az első az energiatárolók mérete (azaz az üzemanyagtartály), a második pedig az, hogy ezt az energiát hogyan hasznosítják (azaz mérföld/gallon).
Az energetikai kapacitást befolyásolhatja a korábbi táplálkozási előzmények, valamint a tápanyagok tárolt tartalékokká történő átalakulásának relatív hatékonysága. Az energiafelhasználást ugyanúgy számos különféle biológiai tényező befolyásolja, ideértve az anyagcsere igényeket, a készletek átalakítását egy elérhető energetikai pénznemre, valamint az aktív szövetek relatív felhasználási hatékonyságát (oxidációs kapacitása). Az energetikai igények újraelosztása kritikus szempont a stresszreakciók fellendítésében, és ezek a válaszok a homeosztatikus kihívások enyhítésére szolgáló biológiai prioritásokat tükrözik.
Drosophilában, valamint sok más metazoánban az éhezés hiperaktív viselkedést vált ki. Ez a mozgásváltozás általános adaptív jelentőséggel bír, mivel megkönnyíti a szervezet eltávolítását a stressz forrásából, vagy az éhezés speciális eseteiben elősegíti a táplálékkal való viselkedést. Az éhezés nyilvánvalóan az energiatárolók kimerüléséhez is vezet, amelyet súlyosbít a megnövekedett aktivitási szint és az ezzel egyidejűleg magasabb metabolikus igény. Nyilvánvaló, hogy a megnövekedett aktivitás kiváltja az energiatartalékok veszteségét, de fordítva is igaz lehet - vagyis az, hogy a mozgás mértékét végső soron az energia elérhetősége szabályozza. Ha ez a helyzet, akkor feltételezhetjük, hogy a perifériás szövetek szenzoros információkat közvetítenek azoknak a központi régióknak, amelyek kontrollálják a mozgás viselkedését. Alternatív megoldásként az éhezés független változásokat indukálhat az energia mobilizálásában és a mozgásban.
A szelekciós elemzés betekintést nyújt a mögöttes genetikai összetevőkbe is, amelyek kvantitatív vonás lokuszok (QTL) vagy mikroarray elemzések segítségével könnyen kivizsgálhatók. Az éhezési körülményeknek kitett állatok transzkripciós elemzése általános immuncsökkenést mutat az immunitásban működő gének átirataiban (Harbison et al., 2005). Ezen eredmények alátámasztására a parazitált Drosophila túlérzékeny az éhezési és kiszáradási stresszekre (Hoang, 2001). Ez arra utal, hogy az energiák elterelésének elmulasztása az immunrendszerrel kapcsolatos funkcióktól hátrányosan befolyásolja a túlélést ilyen körülmények között. Ezt támasztja alá az a megfigyelés is, miszerint az immunrendszer krónikus stimulálása Drosophilában csökkenti az élettartamot (Libert et al., 2006). Hasonlóképpen, a mikroarray elemzés fokozott expressziót mutat be az energia mobilizáció metabolikus folyamatain belül működő különféle transzkriptumokban (Harbison et al., 2005). Ezek az eredmények alátámasztják az energiaraktárak és -használatok központi szerepét, mint az éhezés okozta módosítás kritikus célpontját.
- Nephrolithiasis - áttekintés a ScienceDirect témákról
- Nephrosclerosis - áttekintés a ScienceDirect témákról
- Skinfold - áttekintés a ScienceDirect témákról
- Nátriummérleg - áttekintés a ScienceDirect témákról
- Pihenő energiaköltségek - áttekintés a ScienceDirect témákról