A zsírszövet súlyban betöltött szerepe visszanyerhető a fogyás után
P S MacLean
Orvostudományi Tanszék, Endokrinológiai, anyagcsere és cukorbetegség osztály, Anschutz Egészségügyi és Wellness Központ, Colorado Egyetem Orvostudományi Kar, Aurora, Colorado, USA
J A Higgins
Orvostudományi Tanszék, Endokrinológiai, anyagcsere és cukorbetegség osztály, Anschutz Egészségügyi és Wellness Központ, Colorado Egyetem Orvostudományi Kar, Aurora, Colorado, USA
E D Giles
Orvostudományi Tanszék, Endokrinológiai, anyagcsere és cukorbetegség osztály, Anschutz Egészségügyi és Wellness Központ, Colorado Egyetem Orvostudományi Kar, Aurora, Colorado, USA
V D Sherk
Orvostudományi Tanszék, Endokrinológiai, anyagcsere és cukorbetegség osztály, Anschutz Egészségügyi és Wellness Központ, Colorado Egyetem Orvostudományi Kar, Aurora, Colorado, USA
M R Jackman
Orvostudományi Tanszék, Endokrinológiai, anyagcsere és cukorbetegség osztály, Anschutz Egészségügyi és Wellness Központ, Colorado Egyetem Orvostudományi Kar, Aurora, Colorado, USA
Absztrakt
Bevezetés
Az Egyesült Államokban a felnőttek több mint 60% -a és a gyermekek közel 20% -a túlsúlyos vagy elhízott (1,2). A súlycsökkentő stratégiák csak átmenetileg hatékonyak a legtöbb ember számára, mivel a fogyást megkísérlő egyének túlnyomó többsége nem képes 10% -os csökkenést elérni és fenntartani egy év alatt (3). A lefogyott súly több mint egyharmada hajlamos visszatérni az első évben, a többség pedig 3-5 éven belül visszanyerhető (4,5). Számos okot javasoltak a magas visszaesési arányra (5,6), de jelentős bizonyíték áll rendelkezésre a fogyás utáni testsúly visszanyerésére irányuló biológiai törekvésre (7,8). Jelen áttekintés célja összefoglalni a fehér zsírszövet hozzájárulását ehhez a biológiai hajtáshoz, és megvitatni, hogy a celluláris és metabolikus jellemzőinek változásai hogyan segíthetik elő a súly visszanyerését.
A tömeg visszaszerzésének biológiai törekvése
A testtömeg biológiai szabályozása komplex visszacsatolási hurkot foglal magában az agy és a periféria között. Az agy jeleket kap a perifériáról a hosszú távú energiaraktárak (azaz a zsírszövet triglicerid) és a rövid távú tápanyagok elérhetősége (azaz a keringő tápanyagok azonnali elérhetősége) vonatkozásában, és ezen integrált jelek alapján úgy állítja be az energiaháztartást, hogy mind a hosszú távú és az energia homeosztázis rövid távú célkitűzései. Ez a visszacsatolási rendszer akkor alkalmazkodik, ha az energiafogyasztást kognitív módon (embereknél) vagy erőteljesen (állatmodellekben) korlátozzák.
Ennek az energiahiánynak az alapvető megértése, amelyet kizárólag a biológiai nyomás diktál, az étrend okozta elhízás (DIO) modellekben a testsúly visszanyerésének preklinikai tanulmányaiból derült ki. Az energiahiányt a fenntartó-relapszusos átmenetnél előre jelezhető módon befolyásolja az étrend összetétele (12), a súlyvesztés időtartama a fogyás után (10) és a fizikai aktivitás szintje (13). A súly visszanyerése, amelyet kizárólag ez a biológiai nyomás hajt, tükrözi az elsőrendű növekedési görbét (4,11,13), így az elhízáshoz való visszatérés előrehaladtával az energiahiány csökken. Mint ilyen, az energiarés nagysága a súlycsökkenés utáni legalacsonyabb súlynál a legnagyobb (9,11,13). Ezen túlmenően ez az energiahiány nem oszlik el a súlymegőrzés idővel. A vizsgálatok inkább azt mutatják, hogy az energiahiány nagysága fokozatosan növekszik, minél tovább fenntartja az állat csökkentett súlyát korlátozott energiájú étrenddel (10). Ezeknek a megfigyeléseknek az a következménye, hogy a biológiai nyomás az idő múlásával erősödhet a testsúly fenntartása és az elveszített súly mennyisége mellett.
A fehér zsírszövet a homeosztatikus rendszer kritikus csomópontja, amely ellenőrzi a testsúlyt, és különösen fontos szerepet játszik a fogyás visszaszerzésének biológiai törekvésében. Az elmúlt évtizedekben a zsírszövetet dinamikus, multifunkcionális szervként ismerik el, számos különféle sejttel (14,15). A tárolt energia nagy részét trigliceridként tartalmazza, amelyről azt gondolják, hogy ez a hosszú távú energia homeosztázis szabályozásának elsődleges célzott paramétere. Az adipocita az energia hosszú távú tárolásának elsődleges célját szolgálja, és a súlygyarapodás, -vesztés és -visszanyerés során az adipocitáknak és támogató sejtjeiknek jelentős mennyiségű átalakításon kell átesniük a tárolt energia nyereségének vagy veszteségének befogadására (16). A visszacsatolási rendszer integrált csomópontjaként a zsírszöveteknek fontos jeleket kell küldenie és fogadnia az agyba és más perifériás szövetekbe és onnan, hogy megfelelően beállítsák a tárolt energia szintjét.
Az adipocita cellularitásának változásai
Adipocita mérete: erősen módosított
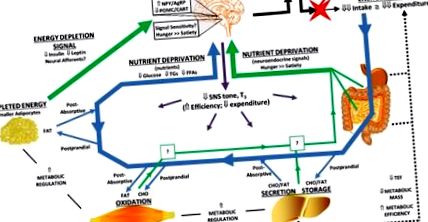
Az adipocita cellularitása a fogyás és a súly visszanyerése következtében változik. A reprezentatív adipocitákat az elhízás összefüggésében, a fogyás és a súly visszanyerése után mutatják be. A súlycsökkenés csökkentené a rezidens adipociták átlagos méretét. A súly visszanyerése mind hipertrófiával, mind hiperpláziával járhat. Az egyes metabolikus kontextusokban bemutatjuk azokat a változásokat a neuroendokrin inputokban (SNS tónus és T3), amelyek hozzájárulhatnak a testsúlycsökkenéshez való adaptív válaszhoz. Hasonlóképpen, minden anyagcsere-kontextusban bemutatjuk a tárolt energiát (leptint és inzulint) tükröző hosszú távú zsírszignál szekréciójának változását. Végül a tápanyagok elérhetőségére gyakorolt szisztémás hatást a glükóz, a trigliceridek (TG) és a szabad zsírsavak (FFA) relatív fluxusaként mutatjuk be. Mind a hosszú távú (leptin), mind a rövid távú (tápanyagok és azok helyettesítő szignáljai) érzékelését a hipotalamusz és a hátsó agy szabályozná az étvágy és az anyagcsere szükségletei szempontjából.
Adipocita szám: egyirányúan módosítva
A súlycsökkenés nem vezet észrevehető változáshoz a zsírszövetben lévő adipociták számában (11,13,17–19) (2. ábra). A normális, egészséges egyénben az adipocyták száma a felnőttkorban viszonylag állandó marad (20), de vannak olyan körülmények, amelyekben az adipocyták száma különösen a zsírraktárakban növekedhet. A súlycsökkenés és a visszanyerés rágcsáló paradigmájában végzett vizsgálataink azt sugallják, hogy az elhízás visszaesése alatti anyagcsere-körülmények biztosíthatják azokat a körülményeket, amelyek elősegítik a hiperpláziát. A relapszus folyamatának kezdetén nagyon kicsi populáció megjelenését figyeltük meg (2). Az SNS megállapította a zsírszövetek metabolikus állapotára és cellularitására gyakorolt hatásait (74, 75), és az SNS-tónus csökkenése ebben a szövetben magyarázhatja az anyagcsere-állapot elmozdulását, ami elősegíti a felvett energia felvételét és lerakódását, valamint a hiperpláziát. Más vizsgálatok azt mutatják, hogy mind a preadipocyták, mind az adipocyták hasonló módon reagálnak a pajzsmirigy-stimuláló hormonra (TSH) és a pajzsmirigyhormonokra (76–80). Az SNS és a pajzsmirigyhormonok egyaránt gátló hatást gyakorolnak a preadipocita proliferációra és stimuláló hatással vannak a preadipocita differenciálódásra. Mint ilyen, az SNS-tónus és a pajzsmirigy-tengely aktivitásának csökkenése a testsúly fenntartása során megengedő körülményeket teremthet a preadipocita proliferációhoz, míg ezen neuroendokrin inputok visszafordítása a súly visszanyerése alatt a hiperplázia mögött állhat. Míg ezek a neuroendokrin inputok elfogadható magyarázatot nyújtanak mind a metabolikus, mind a celluláris alkalmazkodásra a fogyás és a visszanyerés során, tényleges hozzájárulásuk a zsírszövetek adaptív válaszához további tanulmányokat igényel.
Zsírjelek a hosszú távú energiatárolók számára
Ami megnehezíti a leptin és az inzulin „zsírjelekként” játszott szerepét, az az, hogy kapcsolatuk az adipozitással csak az energiaegyensúly alatt marad fenn, és az összefüggések csak a hormonok éheztetett szintjére vonatkoznak. Energia-egyensúlyhiány bekövetkezésekor a leptin és az inzulin tükrözi a zsírszövet metabolikus állapotát (anabolikus vagy katabolikus), mivel energiát rak le vagy mozgósít. A túltáplálás növeli a keringő leptin és inzulin szintjét (93), és a súly visszanyerése alatt fennálló tartós túladagolással mind a leptin, mind az inzulin jóval a súly teljes visszanyerése előtt megszűnik (7). Emiatt a leptin és az inzulin önmagában nem úgy tűnik, hogy fenntartaná az energia kimerülésének jelét, mivel a súly helyreáll.
A tápanyagok rendelkezésre állása, mint a felesleges energia tárolásának képessége
A testsúly dinamikus szakaszának „tápanyag-clearance” hipotézise visszanyeri
Ez a hipotézis azt sugallja, hogy az étvágy és az elfogyasztott energia közötti energiarés továbbra is fennáll a súly visszanyerése során, a zsírszövet azon képességének függvényében, hogy tisztítsa és tárolja a felesleges energiát (7. ábra) (2. ábra). A visszaesés korai szakaszában a zsírszövet azon képessége, hogy megtisztítsa a felesleges energiát, a tápanyagok elfogyasztásának és felszívódásának sebességével áll szemben. A súly visszanyerésének előrehaladtával az adipociták mérete fokozatosan növekszik, és a felesleges energia tisztítására való képességük csökken. A glükóz és a TG-k kirándulásai nagyobbak lesznek, és az FFA szuppressziója dinamikus (étkezés utáni) anyagcsere-állapotok alatt fokozatosan gyengül. Amint az adipociták elérik a méret kritikus küszöbét és a tárolt energia maximális kapacitását, csökken a súly visszaszerzésének sebessége. Mivel a súlycsökkenés előtti súly ismét eléri, vagy meghaladja, ha adipocita hiperplázia lépett fel, a keringő tápanyagok éhomi és étkezés utáni szintje ismét az inzulinrezisztens állapotban megfigyelt magas szintet tükrözné.
Ez az leegyszerűsített hipotézis integrálja a hosszú távú zsírjeleket, tükrözve a „tárolt energia” szintjét, és a tápanyagok rendelkezésre állásának rövid távú jelzéseivel, amelyek lényegében az „energia tárolásának képességét” tükrözik. Mindkét jel alapvetően a zsírszövetek sejtes és metabolikus profiljában gyökerezik. Fogalmilag a leptin és az inzulin által nyújtott hosszú távú jelek létrehoznák a globális „anabolikus” hangot a hipotalamuszban, a hátsó agyban és a perifériás szövetekben. Ebben az anabolikus kontextusban a keringő tápanyagok és azok helyettesítő neuroendokrin szignáljai fontosabbá válnak étkezés utáni körülmények között és a túlzott táplálkozás kiterjedt rohamai alatt, miközben a súly helyreáll. Ezeknek a hosszú és rövid távú jeleknek a konvergenciája az agy energia homeosztatikus áramköreiben meghatározná az energiahézag nagyságát és tartósságát.
Következtetések
A zsírszövetek a homeosztatikus rendszer kulcscsomópontját jelentik, amely szabályozza a testtömeget. A kalória korlátozásból adódó súlycsökkenés lényeges változásokat eredményez, amelyek a zsírszöveteket elősegítik a bevitt energia felvételére és tárolására. A homeosztatikus rendszer egyéb adaptációival együtt ezek a zsírszövetekben bekövetkező változások jelentős kihívást jelentenek a sikeres fogyás fenntartása szempontjából. A súlycsökkenés tartósan, felesleggel telített módon ébreszti fel a szervezet védelmi rendszerét, és jól összpontosít a szervezet kimerült energiatartalékainak helyreállítására. A sikeres, hosszú távú fogyás megköveteli e biológiai nyomás erősségének és tartósságának felismerését, valamint annak jobb megértését, hogy miként lehet ezeket környezeti, viselkedési és gyógyszerészeti beavatkozásokkal ellensúlyozni. A zsírszövetek és pontosabban az adipociták fontos célpontot jelenthetnek a beavatkozások kialakításában, tekintettel az adaptív válaszban betöltött kritikus szerepükre. A súly visszaszerzésének megakadályozását célzó beavatkozásoknak valószínűleg annyira átfogónak, tartósnak és feleslegesnek kell lenniük, mint azok a biológiai adaptációk, amelyeket megpróbálnak ellensúlyozni.
Összeférhetetlenségi nyilatkozat
A szerzők nem jelentenek összeférhetetlenséget.
- Az aminosav-zsírégető aminosavak szerepe a fogyásban
- Az étrend és a fogyás szerepe a másodlagos hipogonadizmus javításában elhízott férfiaknál vagy
- A vérkémia szerepe a fogyás folyamatában ARCpoint Labs
- Az aerob testmozgás és az étrend szerepe az izmokat súlycsökkenésben
- A Hold fázisainak szerepe a fogyásban • Dzhingarov