Prosztatafibrózis, alsó húgyúti tünetek és BPH
Jose A. Rodriguez-Nieves
Sejt- és molekuláris biológiai program, Michigan Egyetem, 2966 Taubman Medical Library, Ann Arbor, MI 48109-0619, USA
Jill A. Macoska
Biológiai Tanszék, Massachusettsi Egyetem, 100 Morrissey Boulevard, Boston, MA 02125-3393, USA
Absztrakt
Az alsó húgyúti tünetek (LUTS) - a spektrum rendellenességét alkotják, amely magában foglalja a gyenge áramlást, a nokturiát és a hiányos ürítés, valamint az időszakos vagy tétova vizelés érzetét - az alsó húgyúti diszfunkcióra (LUTD) utalnak. A LUTD egy progresszív betegség, amely húgyhólyag-diszfunkcióhoz vezethet, ha nem kezelik vagy hatástalanul kezelik. A következmények magukban foglalják a vizeletretenciót, a visszatérő UTI-t, a húgyhólyag számát és végül a vesekárosodást. A prosztatát bevonó LUTD mind az öregedéssel, mind a gyulladással jár. Az öregedésből, fertőzésből vagy más gyulladásos betegségből (például 2-es típusú diabetes mellitusból) eredő szövetgyulladás epidemiológiailag összefügg a szöveti fibrózis későbbi kialakulásával több szervrendszerben, beleértve a prosztatát is. A legújabb tanulmányok azt mutatják, hogy az alsó húgyutak szöveti fibrózisa összefügg a LUTD-vel, és arra utalnak, hogy a fibrózis egy korábban fel nem ismert patobiológia lehet, amely hozzájárul a LUTD-hez. Ezért az antifibrotikus terápiás szereket új megközelítésnek kell tekinteni a LUTD-ben szenvedő férfiak hatékony kezelésében, különösen azokban, akik nem tapasztalnak tartós választ az 5α-reduktáz inhibitorokra vagy az α-adrenerg receptor antagonistákra.
Bevezetés
Az alsó húgyúti tünetek (LUTS) költséges és potenciálisan kritikus orvosi problémát jelentenek az idősödő férfiak milliói számára. Ez a spektrumzavar olyan tüneteket ölel fel, mint a gyenge áramlás, a nokturia, valamint a hiányos ürítés és az időszakos vagy tétova vizelés érzése, amelyek mind az alsó húgyúti diszfunkcióra (LUTD) utalnak. Ha nem kezelik vagy hatástalanul kezelik, a LUTD a hólyag diszfunkciójává válhat, ami vizeletretencióhoz, visszatérő UTI-hez, húgyhólyagkőzethez és végül vesekárosodáshoz vezethet. Az 1–5 LUTD gyakran, bár nem mindig, együtt jár a BPH-val - a prosztata proliferatív, de nem rosszindulatú megnagyobbodása.
A prosztata szövetek műtéti ablációja és az androgén aktivitás (például 5a-reduktáz inhibitorok) vagy a simaizmok kontraktilitásának (például a-adrenerg receptor antagonisták) célzásának orvosi megközelítése felhasználható a LUTD kezelésére. Az Egyesült Államokban az elmúlt 10 évben a műtéti transzurethralis prosztatektómia (TURP) alkalmazása folyamatosan csökkent, valamint a minimálisan invazív technológiák (MIST), különösen a lézeres párologtatás alkalmazásának folyamatos növekedése tapasztalható. 6,7 Egy nemrégiben 1645 LUTS-ben szenvedő kórházi betegnél végzett vizsgálatban a lézeres abláció 4 éves újrakezelési aránya 8,3% volt, szemben a TURP 12,8% -ával. 8 Egy közösségi alapú tanulmány a LUTS jelentős javulásáról számolt be TURP-vel vagy lézeres párologtatással végzett kezelés után, de nem 5a-reduktáz inhibitorokkal vagy α-adrenerg receptor antagonistákkal (amelyek csak stabilizálták a LUTS-t). 9.
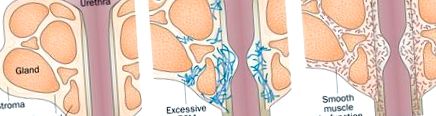
Prosztata patobiológiák, amelyek hozzájárulnak az alsó húgyúti diszfunkcióhoz. A prosztata fibromuscularis stroma által körülvett ductalis mirigyekből áll, amelyek viszont körülveszik a prosztata húgycsövet. a | A ductalis mirigyek és a fibromuscularis stroma külön-külön vagy egyidejűleg hiperproliferálódhatnak, prosztata megnagyobbodást és húgycsőelzáródást okozva. A BPH orvosilag kezelhető az 5α-reduktáz inhibitorokkal, amelyek megakadályozzák a tesztoszteron aktív formájává, dihidrotesztoszteronná történő átalakulását, ami a rendelkezésre álló dihidrotesztoszteron és a prosztata szövetek proliferációjának csökkenéséhez vezet. b | A myofibroblast fenokonverziója és felhalmozódása - és ennek következtében az ECM lerakódása a periurethralis prosztata szövetekben (és esetleg a szomszédos szövetekben) - szöveti merevséget és csökkent húgycső-megfelelést okoz az alsó húgyúti tünetekkel rendelkező férfiaknál. c | A prosztata simaizmai diszfunkcionális kontraktilitást mutathatnak, következményes vizeletürítési diszfunkcióval, amely orvosilag kezelhető az a-adrenerg receptor antagonistákkal (amelyek ellazítják a simaizmokat). Rövidítés: ECM, extracelluláris mátrix.
Gyulladás és LUTD
Prosztata gyulladásos infiltrátum
A gyulladás forrásai
- ▪ Gyulladásos infiltrátum
- ▪ UTI
- ▪ Prostatitis
- ▪ Öregedés
- ▪ 2-es típusú diabetes mellitus
Prostatitis és UTI
A gyulladás és az alsó húgyúti gyulladásos károsodás másik forrása a prosztatagyulladás. Számos epidemiológiai tanulmány kimutatta, hogy összefüggés van a prosztatagyulladás és a későbbi LUTD kialakulása között. Az egészségügyi szakemberek nyomon követési vizsgálatának adatai szignifikáns összefüggést mutattak a gonorrhoealis fertőzés története vagy a fiatal betegség kialakulása között (15 évesek. Az Olmsted megyei férfi egészségügyi tanulmány kimutatta, hogy az orvos által diagnosztizált prosztatagyulladásban szenvedő férfiaknál szignifikánsan nagyobb az esély a prosztatizmus, a BPH, a LUTS kialakulására., vagy megnagyobbodott prosztata (P 16, 17, összesen 10 617 férfit érintő öt vizsgálat összesített adatai azt sugallják, hogy a prosztatagyulladásról korábban beszámoló férfiaknál jelentősen megnő a BPH, a LUTS és a prosztatarák kialakulásának kockázata. 18 UTI szintén társul férfi LUTD. Egy 208 bakteriuriában szenvedő beteg egyik vizsgálatában 54% -uknál diagnosztizálták az UTI-t, és ezek a betegek ürességi diszfunkciót mutattak ki, ami a dysuria magasabb arányában (P = 0,0001), a sürgősségben (P = 0,0001) és a gyakoriságban (P = 0,0001; 1. háttérmagyarázat
Az öregedéssel járó gyulladás
A prosztata gyulladása az öregedés normális folyamatából is származik. Az interleukin-8 és a szorosan kapcsolódó C-X-C motívum kemokin (CXCL) 5 jelentősen nagyobb koncentrációját választják ki az idősebb férfiak prosztatáiból tenyésztett stromális fibroblasztok, mint a fiatalabb férfiakhoz. 20–22 Ezenkívül az interleukin-8, CXCL5, CXCL1, CXCL6 és CXCL12 szekréciója az öregedő prosztata stroma által in vitro proliferatív válaszokat indukál mind a hám, mind a stroma prosztata sejtjeiből. 21–23
Más vizsgálatok kimutatták, hogy a miofibroblasztban gazdag reaktív sztróma a hiperplasztikus, diszplasztikus és neoplasztikus asszociált prosztata stromát jellemzi, 33,34 BPH csomók fokozott epitheliális CXCL8 immunreaktivitást mutatnak (általában reaktív stromához társulva), 33 CXCL8 indukálja a fibroblastok differenciálódását a myof A keratinocita eredetű kemokin (a CXCL8 egér homológja) túlexpresszálása egér prosztata epitheliumában hiperplasztikus prosztata epitheliális acinit eredményezhet (jellemzően periacináris reaktív stromával társulva). 35 Ezenkívül a CXCL5, CXCL8 és CXCL12 elősegítik a normális prosztata fibroblasztok in vitro miofibroblasztokká történő átmenetét. 36 Összességében ezek az adatok arra utalnak, hogy az öregedő gyulladásos mikrokörnyezet elősegítheti a myofibroblast felhalmozódását és a prosztata szöveti fibrózisát. Így társbetegség hiányában a „normális” öregedési folyamatok elegendőek lehetnek az alsó húgyúti szöveti architektúra fibrotikus változásainak és az ebből következő obstruktív ürítési tünetek elősegítéséhez (1. háttérmagyarázat).
A cukorbetegséggel járó gyulladás
A negyedik gyulladásforrás, amely potenciálisan befolyásolhatja az alsó húgyutakat, a 2-es típusú diabetes mellitus (T2DM). Számos közelmúltbeli epidemiológiai vizsgálat adatai szerint a LUTD a T2DM-ben szenvedő férfiak körében gyakrabban fordul elő, mint az egészséges kontrolloknál. 37 klinikailag diagnosztizált BPH-ban szenvedő 8856 férfi között a diabetes mellitus (13% -os prevalencia) jelenléte a LUTS megnövekedett súlyosságával járt, ami jobban befolyásolta az ürítési funkciót, mint a tárolási funkciót. A BPH-ban és T2DM-ben szenvedő betegeknél szignifikánsan magasabb volt az alapszintű nemzetközi prosztata tüneti pontszám (IPSS; 20,5 ± 0,2) és szignifikánsan alacsonyabb a maximális vizeletáramlás (Qmax; 10,4 ± 0,2), mint a BPH-ban szenvedőknél, de T2DM nélkül (18,6 ± 0,1 és 11,5 ± 0,1, ill. P 38 Valójában azt feltételezik, hogy a T2DM-nek és a LUTD-nek ugyanazon gyulladásos patogenezisük van, mivel sok, a gyulladásban szerepet játszó citokin kapcsolódik mindkét állapothoz.
Állatmodellekben biológiailag megerősítették a T2DM, a LUTD iniciáció és a progresszió közötti kapcsolatot. A magas zsírtartalmú étrenddel (HFD) táplált nyulak metabolikus szindrómát mutattak, amit a hiperglikémia és a glükóz-intolerancia, a megnövekedett szérum triglicerid- és koleszterinszint, valamint az átlagos artériás nyomás (MAP) és a zsigeri zsírszövet (VAT) bizonyít. 40 Ezeknek a nyulaknak a hólyagelváltozásai is kialakultak (beleértve a fibrózist, a hipoxiát és az alacsony fokú gyulladást) a csökkent húgyhólyag-megfeleléssel együtt. 40,41 A HFD tehát metabolikus szindrómához, T2DM-hez, gyulladáshoz és vizeletürítési diszfunkcióhoz társult. Hasonló vizsgálatok azt mutatták, hogy a HFD-vel táplált SAMP6 és AKR/J egerek étrend által kiváltott elhízást és T2DM-t fejlesztettek ki a megnövekedett VAT, prosztata gyulladás, prosztata és húgycső szöveti fibrózisával és vizeletürítési diszfunkcióval párhuzamosan. 42 Összességében ezek a vizsgálatok azt mutatják, hogy az alsó húgyúti gyulladás epidemiológiailag és biológiailag összefügg a szöveti fibrózissal és a LUTD-vel (1. háttérmagyarázat).
Prosztatikus fibrózis
Az öregedés, a fertőzés és más gyulladásos megbetegedések által okozott szövetgyulladás epidemiológiailag összefügg a szöveti fibrózis későbbi kialakulásával több szervrendszerben, olyan állapotokhoz vezetve, mint a hasnyálmirigy diszfunkciója, 43,44 krónikus obstruktív tüdőbetegség, 45,46 cirrhotás alkoholmentes zsíros májbetegség, 47,48 és Crohn-betegség. 49–51 Mechanikailag a fibrózis a gyulladás után folyik le (2. ábra), és gyulladás által indított, rendellenes sebgyógyulási folyamatnak tekinthető, amelyet myofibroblast felhalmozódás, kollagén lerakódás, extracelluláris mátrix (ECM) átalakítása és megnövekedett szöveti jellemzők jellemeznek. merevség. 36,51–54 A szöveti fibrózis károsítja a szerv működését azáltal, hogy a normál szövetet erősen kollagénizált hegszövetre cseréli, növeli a szövetek merevségét (ezáltal csökkenti a szövetek rugalmasságát és megfelelőségét), megzavarja vagy megszünteti a szövetek normális beidegződését és érrendszerét.
A gyulladás és a fibrózis hozzájárulása az alsó húgyúti diszfunkcióhoz (LUTD). Az UTI, a prosztatagyulladás, az öregedés és a 2-es típusú diabetes mellitus mind a szöveti gyulladás forrása, amely elősegíti az alsó húgyúti fibrózist. A periurethralis szöveti fibrózis, a stromalis vagy epitheliális prosztata proliferáció és a simaizom diszfunkció önmagában vagy kombinációban elősegítheti a férfi LUTD-t. Ez a három patobiológia egyidejűleg fordulhat elő ugyanabban a prosztata mirigyben.
Seb aktivált ECM átalakítás
A fibrózis hibás sebgyógyulási folyamatnak tekinthető, amelyet a myofibroblasztok aktiválása és felhalmozódása jellemez, amelyek számos szövetben átmenetileg termelődnek a normális sebválasz részeként. Számos sejttípus, köztük fibroblasztok, periciták, fibrociták és mezencimális sejtek, képesek lehetnek differenciálódni miofibroblasztokká. 55 A miofibroblaszt-differenciálódás közös jellemzői az a-simaizom aktin (α-SMA) és az I. típusú kollagén expressziója, amely a miofibroblaszt szekretált ECM nagy alkotóeleme. Az α-SMA-t expresszáló miofibroblasztok fokális tapadást képeznek a környező kollagénnel megnövelt ECM-mel, és ezeknek a miofibroblasztoknak az összehúzódása biztosítja a seb összehúzódásához és bezárásához szükséges mechanikai erőt. Az ezt követő sebzárás csökkenti a myofibroblasztok mechanikai terhelését - amelyet az α-SMA potenciálisan érzékel, és amelyről azt gondolják, hogy mechanosenzoros fehérje -, ami a fokális adhéziók feloldódásához, az α-SMA szétszereléséhez, és végül a myofibroblast apoptózisához és a sejthalálhoz vezet. 53,54 Ha a seb nem záródik le, a myofibroblastok nem kapják meg a mechanikai jelet, hogy apoptózissá váljanak, és tovább halmozódnak fel és rakják le az ECM-et, ezáltal a normál szövetet fibrotikus szövetekkel helyettesítik.
A prosztata sztromális fibroblasztok indukálhatók a fibrózissal társult 1 és 3 kollagén és az α-SMA expresszálására, valamint teljes funkcionális miofibroblaszt fenokonverzión átesnek a TGF-β-kanonikus profibrotikus fehérje vagy a CXCL CXCL5, CXCL8 és CXCL12 (akár exogén TGF-β1 hiányában). 36 Ezenkívül a CXCL12 által közvetített miofibroblaszt fenokonverzió teljesen megsemmisíthető a CXCR4 CXCR4 receptor gátlásával. Ezek a megállapítások azt sugallják, hogy a CXCL-ek, amelyek gyulladásos fehérjéket tartalmaznak, amelyekről ismert, hogy magasan expresszálódnak az öregedő prosztatában, hatékonyan és teljes mértékben közvetíthetik a myofibroblast fenokonverziót, és ezért elősegíthetik a prosztata szöveti architektúrájának fibrotikus változásait, amelyek a hím férfiak fejlődésével és progressziójával járnak LUTD. 36
Periurethralis ECM lerakódás és fibrózis
Myofibroblast fenokonverzió és a prosztata fibrózisának megindulása. a | Az egészséges prosztata szövet különféle sejttípusokból áll, beleértve a fibrocitákat, fibroblasztokat, hámsejteket és endoteliális sejteket, valamint más, itt nem látható sejteket (például neuronok és leukociták). b | Ezen sejttípusok közül sok olyan prekurzor sejtként működhet, amelyek myofibroblast fenokonverzión mennek keresztül, amikor profibrotikus ingereknek vannak kitéve. A miofibroblasztok felhalmozzák és lerakják a túlzott ECM-et, amely a normál szövetet merev, nem kompatibilis fibrotikus szövetekkel helyettesíti. Rövidítés: ECM, extracelluláris mátrix.
A fibrózis terápiás célzása
Az ellátás színvonala
Számos klinikai vizsgálat kimutatta, hogy azok a betegek, akik a prosztata sugárterápiáján estek át - ez az eljárás szöveti fibrózist vagy húgycső szűkületeket indukálhat 57 - kimutatják a LUTS jelentős csökkenését az α-adrenerg receptor antagonistákkal végzett kezelés után. 58 Állatkísérletek kimutatták, hogy az α-adrenerg receptor agonista fenilefirinnel kezelt patkányok ventrális prosztatáit intersticiális fibrózis, gyulladás, neoangiogenesis és a kollagén de novo szintézise befolyásolja (ami desmoplasztikus reakcióra utal). 59 Ezzel szemben más vizsgálatok kimutatták, hogy az α-adrenerg receptor antagonista doxazozinnal kezelt felnőtt Wistar patkányok ventrális prosztatái megemelkedett kollagén és kollagén fibrillák szintjét tartalmazzák a kezeletlen kontrollokhoz képest. 60 A-adrenerg receptor antagonista ismert, hogy a vaszkuláris és simaizom sejteket célozza meg az alsó húgyúti traktusban. Azonban a miofibroblasztok, mint a simaizomsejtek, összehúzódnak, 55 és további munkára van szükség annak meghatározásához, hogy a miofibroblasztok az alsó húgyutak simaizomsejtjeihez hasonló módon reagálnak-e az α-adrenerg receptor antagonistákra.
Számos tanulmány dokumentálta a prosztata szövetének felépítésében bekövetkezett szövettani változásokat - beleértve a megnövekedett gyulladásos infiltrátumot és fibrózist - az androgén-deprivációs terápia (ADT) után. 61–63 A BPH vagy LUTS kezelésére rövid vagy hosszú távú 5α-reduktáz gátló terápiával kezelt férfiak prosztata szöveteinek vizsgálatára még nem végeztek vizsgálatokat. Tekintettel azonban a szöveti fibrózis és a LUTD közötti kapcsolatra, az ilyen vizsgálatok indokoltak. Ha az ADT myofibroblast fenokonverzióval és fibrózissal volt összefüggésben a nem malignus prosztata szövetekben, az ilyen kezelés valóban hozzájárulhat a BPH és a LUTS progressziójához néhány férfiban.
Antifibrotikus szerek
Összefoglalva, az öregedésből, fertőzésből vagy más gyulladásos betegségből eredő szövetgyulladás (például T2DM) a prosztata szöveti fibrózisának későbbi kialakulásával jár. A periurethralis prosztata szöveti fibrózis viszont összefügg a LUTD-vel, ami arra utal, hogy a fibrózis egy korábban fel nem ismert patobiológia lehet, amely hozzájárul a LUTD-hez. Ezért az antifibrotikus terápiás szereket új megközelítésnek kell tekinteni a LUTD-ben szenvedő férfiak hatékony kezelésében, különösen azokban, akik nem tapasztalnak tartós választ az 5α-reduktáz inhibitorokra, az α-adrenerg receptor antagonistákra vagy a műtéti ablációra.
Lábjegyzetek
Versenyző érdekek
A szerzők kijelentik, hogy nincsenek versengő érdekeik.
- Természetes megkönnyebbülés kutyája húgyúti fertőzései miatt. Modern kutya magazin
- Nephrogén Diabetes Insipidus - Vese- és húgyúti rendellenességek - Merck Manuals Consumer Version
- A 3. stádiumú betegeknél a 4. stádiumú májfibrózishoz képest alacsonyabb a gyakorisága, és hosszabb az idő
- Vese-glükózuria - vese- és húgyúti betegségek - Merck Manuals Consumer Version
- Tünetek; A hólyagszabályozás problémáinak okai (vizeletinkontinencia) NIDDK