CP 55,940
Kapcsolódó kifejezések:
- Tetrahidrokannabinol
- Kannabinoid
- Agonista
- Kannabinoidok
- WIN 55,212-2
- Dexanabinol
- Cannabinoid 1 receptor agonista
- Ligand
- Cannabinoid 1 receptor
Letöltés PDF formátumban
Erről az oldalról
Neuroimmun jelzés a kábítószer-akciókban és függőségekben
Guy A. Cabral, Melissa Jamerson, a Neurobiology International Review-ban, 2014
3 immunmodulációs és kannabinoid receptorok
Tanulmányok, amelyekben szintetikus kannabinoid vegyületeket, például CP-55,940, HU-210, WIN 55,212, JWH-015, ACEA, SR141716A és SR144528 (8.1. Ábra) alkalmaztak, fontos betekintést nyújtottak a funkcionális relevanciába és a hatásmechanizmusba: mely THC gyakorolja az immunrendszerre gyakorolt hatását. Ezen túlmenően ezek a kollektív vizsgálatok alapot szolgáltak az emlős agy és a perifériás nemneuronális szövetek specifikus kötőhelyeinek azonosításához, amelyekről ma már felismerték, hogy a kannabinoid receptorokat képviselik (Matsuda, Lolait, Brownstein, Young és Bonner, 1990; Munro, Thomas, És Abu-Shaar, 1993). A mai napig két olyan kannabinoid-receptort azonosítottak, amelyek megfelelnek a szigorú farmakológiai és molekuláris kritériumoknak (8.2. Ábra). Ezek közül az első, az 1-es típusú kannabinoid receptor (CBR1) egy szerpentin, hét transzmembranális, G fehérjéhez kapcsolt receptor, amelyről radioligandumkötés és in situ mRNS hibridizáció során megállapították, hogy az agyban eloszlik, és főleg a kisagy, agykéreg, hippocampus, bazális ganglionok és gerincvelő (Herkenham et al., 1990; Matsuda et al., 1990; Westlake, Howlett, Bonner, Matsuda és Herkenham, 1994). A CB1R megtalálható a herékben (Gerard, Mollereau, Vassart és Parmentier, 1991), és kisebb mértékben más szövetekben és sejtekben is. A THC-nek tulajdonított pszichotrop hatások ennek a receptornak az aktiválásának köszönhetők (Agarwal és mtsai., 2007; Kunos, Osei-Hyiaman, Batkai, Sharkey és Makriyannis, 2009).
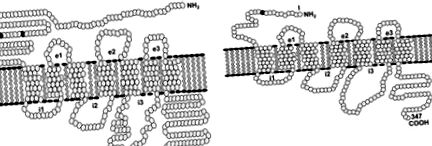
8.2. Ábra A CB1R és a CB2R vázlatos ábrázolása. (A) Egér CB1R: A szilárd körök feltételezett glikozilezési helyeket jelölnek az aszparagin 78. és 84. maradványainál. Az extracelluláris és intracelluláris hurkok e1, e2 és e3, valamint i1, i2 és i3. (B) Egér CB2R: A szilárd kör feltételezett glikozilezési helyet jelöl a CB2 11. aszparagin maradékánál. Az extracelluláris és intracelluláris hurkokat e1, e2 és e3, valamint i1, i2 és i3 jelöljük. A különböző emlősfajok CB1R-ei nagyfokú hasonlóságot mutatnak. A CB2R nagyobb fajok közötti különbségeket mutat az egér CB2R levezetett aminosav-szekvenciájával, amely 60 szermaradékban különbözik az emberétől (82% hasonlóság) (Shire és mtsai, 1996).
B panel: Cabral és Griffin-Thomas (2008) .
Az immunrendszer sejtjeiben és szöveteiben azonosítottak egy második szerpentint, hét transzmembranális, G-fehérjéhez kapcsolt kannabinoidreceptort, a 2-es típusú kannabinoid-receptort (CB2R) (Munro és mtsai., 1993). Ez a receptor körülbelül 44% aminosav-hasonlóságot mutat a CB1R-hez. A CB2R szintje a különböző immunsejtpopulációk között változik, a B-limfociták expresszálják a legmagasabb szintet, majd makrofágok, monociták, NK-sejtek és polimorfonukleáris sejtek következnek ebben a sorrendben (Galiegue et al., 1995; Schatz, Lee, Condie, Pulaski És Kaminski, 1997). A korai vizsgálatok azt mutatták, hogy a CB2R eloszlása a perifériás nem neuronális helyekre korlátozódott. Azonban ma már felismerték, hogy ezt a receptort a központi idegrendszerben található immun-kompetens sejtek különböző alcsoportjai expresszálják (Cabral & Marciano-Cabral, 2005; Carlisle, Marciano-Cabral, Staab, Ludwick és Cabral, 2002; Carrier et al., 2004; Fernandez-Ruiz és mtsai, 2007; Nunez és mtsai, 2004; Ramirez, Blazquez, Gomez del Pulgar, Guzman és de Ceballos, 2005). A THC-nek tulajdonított immunmoduláló hatások többsége a CB2R aktiválásához kapcsolódik.
Az intraokuláris nyomás kannabinoid-szabályozása: Emberi és állatkísérletek, sejtes és molekuláris célok
Nem klasszikus
CP-55,940
A nem klasszikus, biciklusos kannabinoidokat a CP-55 940 prototípusú vegyület képviseli. Ez a vegyület teljes agonistaként viselkedik mind a CB1, mind a CB2 esetében (Howlett és mtsai, 2002; Pertwee, 1999; Pertwee és mtsai, 2010). Legalább két vizsgálatban a CP-55 940 vizes oldatának normotenzív nyulakhoz történő lokális alkalmazása csökkent IOP-értéket eredményezett (Laine et al., 2003; Pate et al., 1998).
Rendellenes kannabidiol
Az abnormális kannabidiol (abn-CBD) a kannabidiol szintetikus regioizomerje. Amikor abn-CBD-t intraperitoneális injekcióval vagy lokálisan patkányon adtak be, az IOP csökkent (Szczesniak et al., 2011).
Kannabinoid farmakológia
Katarzyna Starowicz, David P. Finn, a farmakológia előrehaladásában, 2017
3.1 Az akut fájdalom modellek bizonyítékai
Jelentős erőfeszítéseket tettek a kannabinoid receptor agonisták antinociceptív hatásait közvetítő specifikus agyi régiók tisztázására is (Corcoran, Roche és Finn, 2015). Martin és munkatársai korai munkájában a WIN55,212-2 közvetlen beadása számos különböző agyi régióba, beleértve az amygdala, a thalamus, a superior colliculus és az A5 régiót, bebizonyosodott, hogy antinociceptív a farokcsapás tesztben (Martin, Coffin és munkatársai, 1999). A nem szelektív WIN55,212-2 és HU210 kannabinoid receptor agonisták mikroinjekciója az RVM-be szintén megemelte a farokcsúszás késleltetését patkányokban (Martin, Tsou és Walker, 1998; Meng & Johansen, 2004). Ezenkívül a HU210 hatásait a CB1R antagonista/inverz agonista rimonabanttal való együttes alkalmazással gyengítették (Martin és mtsai., 1998). További bizonyíték az RVM fontosságára az akut fájdalom kannabinoidok által kiváltott csillapításában egy olyan tanulmányból származott, amely bizonyította, hogy az RVM GABAA-receptor agonista által közvetített inaktiválása megakadályozta a szisztémásan alkalmazott WIN55,212-2 antinociceptív hatásait a patkány farokrángási tesztjében ( Meng, Manning, Martin és Fields, 1998). Ezenkívül bebizonyosodott, hogy a WIN55,212-2 RVM-n belüli, farokrángás-teszten belüli alkalmazásának antinociceptív hatása az ON-sejt aktivitásának gátlásával és az OFF-sejt aktivitásának növekedésével jár, a rimonabant blokkolta hatásokkal. (Meng & Johansen, 2004). Az RVM-en belül a nucleus reticularis gigantocellularis pars alfa fontos helynek tűnik a kannabinoid által közvetített antinocicepció számára (Monhemius, Azami, Green és Roberts, 2001).
Kannabinoid farmakológia
Richard Priestley,. David Kendall, a farmakológiai haladásban, 2017
7 A funkcionális szelektivitás mechanizmusai
- Fabaceae - áttekintés a ScienceDirect témákról
- Diétás anyag - áttekintés a ScienceDirect témákról
- Zsíros máj - áttekintés a ScienceDirect témákról
- Zsíros hal - áttekintés a ScienceDirect témákról
- Étrendi minta elemzés - áttekintés a ScienceDirect témákról