Az elhízás és az azzal összefüggő rendellenességek modellezése Drosophilában
Absztrakt
Az elmúlt években az elhízást fő közegészségügyi problémának tekintik, mivel mind gyermekek, mind felnőttek körében fokozott prevalenciát mutat, és számos életveszélyes szövődményhez kapcsolódik, beleértve a cukorbetegséget, a szívbetegségeket, a magas vérnyomást és a rákot. Az elhízás összetett rendellenesség, amely a hajlamosító genetikai és környezeti tényezők közötti kölcsönhatás eredménye. Ezen gén-gén és a gén-környezet kölcsönhatások pontos jellege azonban továbbra sem tisztázott. Itt leírjuk a legutóbbi tanulmányokat, amelyek bemutatják, hogyan lehet a gyümölcslegyeket felhasználni az elhízás hátterében álló mechanizmusok azonosítására és jellemzésére, valamint az elhízással összefüggő rendellenességek modelljeinek felállítására.
Az elmúlt évtizedben az elhízás elterjedtsége riasztó szintet ért el, amelynek eredményeként az Egészségügyi Világszervezet (WHO) globális járványként ismerte el, amely a fejlett és a fejlődő országok lakosságának jelentős részét érinti. A WHO becslései szerint 2015-re 2,3 milliárd túlsúlyos felnőtt lesz világszerte, közülük 700 milliót elhízottnak minősítenek (72). Az elhízás olyan anyagcsere-rendellenesség, amely magában foglalhatja a hiperglikémiát, a magas vérnyomást és a hiperlipidémiát (69, 71), és szorosan összefügg a cukorbetegség, az arteriosclerosis és a szív- és érrendszeri betegségek magas előfordulási gyakoriságával (20, 32). Ezenkívül az elhízás súlyosbítja számos egészségügyi problémát, beleértve, de nem kizárólag, az alvási apnoét, az osteoarthritist, az epeköveket és a rák bizonyos típusait (15, 65). Klinikailag és fiziológiailag az elhízás nagyon heterogén betegség. Az olyan környezeti tényezők mellett, mint a magas zsírtartalmú étrend és a mozgásszegény életmód, a genetikai hajlam vélhetően hozzájárul az energiafogyasztás és a ráfordítás közötti egyensúlyhiányhoz is, amely végül elhízást és az ezzel járó betegségeket eredményez (34). Az intenzív elemzés ellenére az energia-egyensúlyhiányhoz és elhízáshoz vezető etiológiai mechanizmusok nem teljesen ismertek.
Az emberi elhízás Drosophila modelljei
A közelmúltban a nem emlősök genetikai modell organizmusai, beleértve a fonálférgeket, a zebrafish-t és a gyümölcslegyeket, kiváló paradigmákként jelentek meg az emberi betegségek sokféle tanulmányozásához. A Drosophila melanogaster a rendelkezésre álló genetikai eszközök széles skálája, a rövid generációs idő és a nagyméretű, elfogulatlan előremeneti genetikai szűrők végrehajtásának képessége miatt különösen erőteljes modell. Ezenkívül a Drosophila genom elemzése kimutatta, hogy az összes ismert emberi betegséggel kapcsolatos gén ~ 75% -a konzerválódott a legyekben (56).
A közelmúltban a Drosophila-t anyagcserezavarok vizsgálatában alkalmazták, mivel a legyek sok alapvető metabolikus funkcióval rendelkeznek, mint az emlősök, beleértve a cukor homeosztázisának fenntartását, az energiatárolók tárolását és mozgósítását, valamint a táplálékfogyasztás modulálását a táplálkozási jelekre reagálva, és az ezen anyagcsere-folyamatokat szabályozó molekuláris mechanizmusok közül sok konzerválódott. Emellett az emlősök anyagcsere-szerveinek és szöveteinek számos funkcionálisan analóg megfelelője van a legyekben, beleértve a májat, a hasnyálmirigyet és a zsírszövetet (lásd 1. táblázat). Például a légyzsíros test az energia tárolásának helyeként szolgál lipidek és glikogén formájában, hasonlóan az emlős fehér zsírszövetéhez és a májhoz (12). Figyelemre méltó kivétel az, hogy nincs légy egyenértékű barna zsírszövet, amely részt vesz az emlősök energiafelhasználásában. Ebben az áttekintésben összehasonlítjuk a legyek által az energiamérleg fenntartása érdekében alkalmazott mechanizmusokat az emlősökben alkalmazott mechanizmusokkal, és megvitatjuk a Drosophila-modellek hasznosságát az elhízás és az azzal összefüggő rendellenességek tanulmányozásában.
Asztal 1
Az anyagcsere-szövetek konzerválása az emlősök és a Drosophila között
| Emésztés és tápanyagok felszívódása | Gyomor, vékonybél | Középbél |
| Lipid tárolás | Zsírszövet | Kövér test |
| Lipid mobilizáció | Zsírszövet, máj | Kövér test, oenociták |
| Glikogén tárolása | Máj | Kövér test |
| Szénhidrát homeosztázis | Hasnyálmirigy α és β sejtek | Neurosecretory neuronok, corpora cardiaca |
A lipid anyagcsere szabályozása
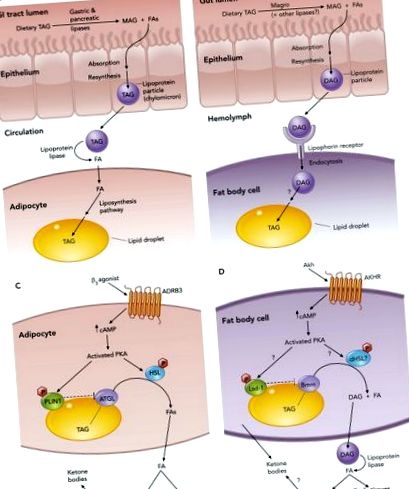
A lipidek a sejteken belül számos döntő funkciót töltenek be. A sejtmembránok nélkülözhetetlen szerkezeti elemei, fontos jelátviteli molekulák, és energiaforrásként szolgálnak a tartós tápanyaghiányos időszakokban is. Mint ilyen, a lipid anyagcsere szabályozása döntő fontosságú a normális fejlődés és a fiziológia szempontjából (25, 38). Ezek a lipid anyagcsere folyamatok komplex mechanizmusokat alkalmaznak, amelyek szabályozzák a lipidfelvételt, transzportot, tárolást és mobilizációt, amelyek konzerválódnak az emlősök és a legyek között (lásd 1. ÁBRA), és diszregulációjuk túlzott lipidtárolást és elhízást eredményezhet.
Lipid anyagcsere útvonalak emlősökben és Drosophila
A lipidek felvétele és szállítása
Az energia-anyagcsere szempontjából kulcsfontosságú szerepet játszik a lipid-anyagcsere zsírsav (FA) ága, amely magában foglalja az FA szintézisét és felvételét, az FA-k triacil-gliceridként (TAG) történő tárolását és az FA-k átalakítását energiatermelés céljából. A gerincesekhez hasonlóan a Drosophila is étrendjéből nyerhet FA-kat, általában TAG formájában, amely szabad FA-kká (FFA-k) és monoacil-gliceridekké (MAG) bomlik le lipázokkal, beleértve a magrót is, amely homológ az emlősök gyomor-lipázjával (63). A mag expressziót közvetlenül a DHR96 árva sejtmag-receptor szabályozza (63), a máj X receptorainak homológja, amely szükséges az egerek trigliceridszintjének szabályozásához (60). A DHR96 mutáns legyek soványak, ellenállnak a magas zsírtartalmú étrend okozta elhízásnak, és érzéketlenek a lipáz inhibitorral történő kezelésre, ami arra utal, hogy az étkezési lipidek lebontásának hibája befolyásolja ezekben a mutánsokban a zsírfelhalmozódást (63).
A bél lumenében található FFA-k és MAG ekkor képesek az enterociták felszívódni és diacil-gliceriddé (DAG) átalakulni, amelyet lipoprotein (más néven lipoforin) részecskékként exportálnak a hemolimfába (a vér légi egyenértéke). A gerincesekkel ellentétben ezek a lipoprotein részecskék a hemolimfában vannak, és nem igényelnek de novo szintézist (12). Ezenkívül úgy gondolják, hogy a rovar lipoprotein részecskéi újrafelhasználható transzfer rendszer, mivel lipidtartalmukat a célszövetekbe juttathatják el anélkül, hogy maga a részecske internalizálódna és lebomlana (12). A Drosophila és az emlősök közötti másik divergencia pont a keringésben domináns semleges lipid: legyekben DAG, emlősökben TAG. Nem ismert, hogy bármelyik acil-glicerid rendelkezik-e különösebb előnnyel. Úgy tűnik azonban, hogy legalább a rovarrendszerben a DAG-t hordozó lipoforinok hatékonyabban működnek újrafelhasználható ingóként, összehasonlítva a TAG-t hordozó fajok lipoforinjaival (51).
A lipidek tárolása és mobilizálása
A lipophorin DAG rakományával a test szöveteibe kerül energiatermelés céljából, vagy a zsír testbe tárolás céljából. Ott megköti a kis sűrűségű lipoprotein receptorokhoz hasonló lipoforin receptorokat (12, 18), és kirakja a DAG-ot, amely átalakul TAG-vé és intracelluláris lipid cseppekben (LD) tárolódik. Az LD-komponensekről számos olyan tanulmány készült, amely bebizonyította, hogy ezek a fehérjék felelősek a TAG-tárolás és a mobilizáció szabályozásáért, és hogy az LD-proteom konzerválódott a legyek és az emlősök között. Ezeket a tanulmányokat számos közelmúltbeli áttekintésben írták le (35–37, 48). Például, ha akár legyek, akár emberek igénylik az energiatermeléshez szükséges lipidek mobilizálását, a lipolitikus jelek az LD-komponensekre hatnak, hogy a lipázok hozzáférhessenek a cseppben lévő tárolt TAG-hoz (lásd az 1. ábrát). Emlősökben a TAG lebomlásából felszabaduló FA-k bejuthatnak a vérbe, és a test szövetei felvehetik őket. Legyekben a TAG bomlástermékeket lipoforinok szállítják DAG-ként, amelyek a szövetekbe jutnak, ahol a lipoprotein-lipáz katalizálja az FA-k felszabadulását a DAG-ból. A zsírsavakat ezután a sejt felveheti β-oxidáció és energiatermelés útján.
Hepatocyta-szerű funkciók a Drosophila FA metabolizmusában
Az emlősmáj vérkoncentrációjának arányában képes felszívni az FA-kat a vérkeringésből, és a túlzott felvétel (például magas lipolízis során) lipidcseppek felhalmozódását eredményezi a hepatocitákban. A megnövekedett FA-felvétel fokozza a ketogenezist is, amely a β-oxidációs termékeket felhasználva oldható ketontesteket állít elő, amelyek felszabadulnak a vérbe, és sok szövet, így az agy és a szív energiaforrásaként is felhasználhatók. Úgy gondolják, hogy ez a folyamat segíti az anyagcsere-üzemanyag eloszlását a különböző szövetekben a negatív energiamérleg időszakaiban.
Legyekben a hepatocita funkciók nagy részét a zsír test végzi. Ezenkívül a zsírtest mögött álló speciális sejtek, úgynevezett oenociták, lipidcseppeket halmoznak fel a májsejtekhez hasonló éhezési körülmények között (26). Nem ismert azonban, hogy ezek a sejtek képesek-e ketogenezishez (ez a funkció kizárólag a zsír testben található meg). Ezen túlmenően az oenocyták működését csak lárváknál vizsgálták, így nem ismert, hogy más vagy kiegészítő funkciókat töltenek-e be felnőtteknél, ahol az anyagcsere programok eltérőek lehetnek.
A szénhidrát-anyagcsere szabályozása
A szénhidrátok az élő szervezetek elsődleges energiaforrása; mint ilyen, a szénhidrát homeosztázis fenntartása fontos szerepet játszik a legyek és az emberek energiamérlegében. Mint korábban említettük, a Drosophilának funkcionálisan analóg hasnyálmirigy-β- és α-sejtjei vannak, amelyek inzulinszerű petideket és adipokinetikus hormont választanak ki, amelyek az inzulin és a glukagon légyváltozatai. Ezenkívül számos jelátviteli út és mechanizmus megőrződött a legyek és az emlősök között. Ezeket a vizsgálatokat számos áttekintés (3, 4, 27, 66) írta le, de itt nem tárgyaljuk őket.
Az energia-anyagcsere CNS-szabályozása
Kimutatták, hogy a központi idegrendszer (CNS) kulcsfontosságú szerepet játszik az energia homeosztázis szabályozásában. Ezzel a szereppel összhangban a legutóbbi Emberi elhízás géntérképének összes génjének ~ 25% -a, és a monogén elhízásba bevont gének majdnem összes génje ismert, hogy az agyban expresszálódnak (55). Ezenkívül a közelmúltban végzett, genomon átívelő asszociációs vizsgálatok több nukleotid polimorfizmust vonnak maguk után több neuronális génben, magas hajlamosságra hajlamosak (40, 67, 73).
Nemrégiben a központi idegrendszerről is kimutatták, hogy szerepet játszik a Drosophila energia-anyagcseréjének szabályozásában. A genom egészére kiterjedő RNSi-szűrőn (53) a ~ 500 gén egyharmada, amelyről kiderült, hogy mindenütt lebontva befolyásolja a tárolt zsírszintet, képes volt megváltoztatni a zsírszintet is, ha expressziójuk kifejezetten csökkent az idegsejtekben. Ezenkívül Al-Anzi és mtsai. (1) szűrést végzett a lipidkészletek szabályozásában részt vevő neuronpopulációk felkutatására, két különálló populációt feltárva. Ezen idegsejt-populációk idegsejt-aktivitásának megváltoztatása az élelmiszer-fogyasztás, a lipid-anyagcsere és a makromolekula-anyagcsere változását eredményezte, amelyet meg lehet fordítani a normál idegsejt-aktivitás helyreállításával. Bár ezek a képernyők a központi idegrendszert bevonják a légy anyagcseréjébe, és annak ellenére, hogy a központi idegrendszer fontos az emlősök energiamérlegében, a molekuláris mechanizmusok még mindig nagyrészt ismeretlenek, és sok Drosophila metabolikus vizsgálatban nem álltak a hangsúly.
Bemenetek a központi idegrendszerbe
A központi idegrendszerről azt gondolják, hogy központi koordinátorként működik, amely figyelemmel kíséri a test energiaállapotát, és elindítja a megfelelő kimeneteket az esetleges zavarok kijavítására az etetési viselkedés és az anyagcsere modulálásával. Ezek a jelek, amelyek a test energiaállapotát közvetítik, a gyomor-bél traktusból, a metabolikus szövetekből származó szignálok és magukból a tápanyagokból, például zsírsavakból és glükózból származó jelek formájában jelentkeznek (33, 59, 62).
Néhány bizonyíték arra utal, hogy a Drosophila agy közvetlenül érzékeli a tápanyagokat. Az agyban a rapamicin (TOR) útjának tápanyag-érzékelő célpontjának aktivitása megváltoztathatja az etetési viselkedést, potenciálisan a táplálkozási állapotra reagálva (57). Ezenkívül bizonyos ízlelő receptorok expresszálódnak az agyi régiók néhány érzéketlen idegsejtjén, amelyek szerepet játszanak az anyagcserében és a táplálkozási magatartásban, ami arra utal, hogy ezek a receptorok potenciálisan működhetnek a tápanyagok érzékelésében ezekben az idegsejtekben (68).
Neuronális jelátviteli hálózat és kimenetek a központi idegrendszerből
A legyeknél az energiaegyensúlyt közvetítő neuronális áramköröket még nem kell teljes körűen jellemezni, de úgy tűnik, hogy az ismert áramkörök egy része összefog az endokrin rendszerben, az agyi régiókban, amelyek beidegzik az etetéshez szükséges izmokat, és az Ilp-t termelő sejtekben (47) . Nagy hangsúlyt fektettek az interneuronális jelzésre az IPC-k számára vagy az IPC-kben történő jelzésre az inzulinszerű peptidek termelésének és/vagy szekréciójának szabályozására, sok tényező azonosításával ezekben a folyamatokban, beleértve az sNPF-et (31, 39), az ERK-t ( 39), S6K (74), JNK (70), szerotonin (43), Cbl (75), tachikininek (6) és Minagy (Mnb) (28).
Az IPC-k több szövetbe küldik a folyamatokat, beleértve az aortát, a gyűrűmirigyet (a légy endokrin mirigyét) és az emésztőrendszer egyes részeit (13, 16), ami arra utal, hogy ezek a célszövetek a központi idegrendszeri kimenetek számára, bár ez a terület további tanulmányokat igényel . A zsír test a keringésbe kerülő Ilps egyik célpontja, és az inzulinreceptor jelátvitel aktiválása hatással van a lipid- és szénhidrát-anyagcserére (66). Például az IPC-ktől érkező jelek a tobi (agyi inzulin célpontja) expresszió szabályozásával szabályozzák a zsírtartalmú cukorraktárakat, amelyek egy olyan α-glükozidázt kódolnak, amely katalizálhatja a glikogén lebomlását (11).
Az etetési magatartás szabályozása a központi idegrendszer másik fontos funkciója az energia homeosztázisban. A legyeknél több olyan mutánst azonosítottak, amelyek változtak az ételpreferenciában és a fogyasztásban, köztük az F neuropeptidet és a hugint, amelyek emlős homológjai az Y neuropeptid és a neuromedin U szerepet játszanak az energia homeosztázisban (áttekintve a 46-os hivatkozásban). Az IPC-k szétválasztják a droszulfakininokat (DSK) is, amelyek az etetési viselkedésben, pontosabban az étel bevitelében és preferenciájában működnek (64). Érdekes módon a DSK-k rokonok a gerinces kolecisztokininnel (CCK) és hasonló szatációs funkciót töltenek be, mint a CCK.
Bár még sok mindent meg kell tanulni a központi idegrendszer szerepéről a legyek energia-anyagcseréjében, ezekben a modellekben nagy lehetőség rejlik, mivel a légygenetikusok számos eszközzel rendelkeznek az idegsejtek működésének tanulmányozására, beleértve a gének és az RNSi-konstrukciók expressziójának specifikus idegsejtpopulációkra történő irányítását., az idegsejtek aktivitásának mérésére és manipulálására szolgáló eszközök, valamint jól kidolgozott viselkedési tesztek, amelyek összességében elősegítik ezen áramkörök funkcionális boncolását.
Az elhízás genetikai elemzése
Az emberi elhízás genetikája
Becslések azt mutatják, hogy a súlyváltozás akár 70% -át genetikai tényezők határozzák meg (8, 14, 30, 41). Ezen tényezők közül néhányat az elhízás ritka monogén formáinak tanulmányozásával azonosítottak, amelyek számos gén mutációit azonosították, ideértve a leptint, a leptin receptort és a melanokortin 4 receptor géneket. Bár ezek a monogén formák a MOP 97871-et teszik ki) G. L. Boulianne számára. I. Trinh a Torontói Egyetem nyílt ösztöndíjának részesül, G. L. Boulianne pedig a kanadai Tier 1 kutatási elnököt tölti be a molekuláris és fejlődési neurobiológia területén.
A szerző (k) nem jelentenek be pénzügyi vagy egyéb összeférhetetlenséget.
- Az általános iskolás gyermekek túlsúlyával és elhízásával kapcsolatos szocio-demográfiai tényezők
- AZ ELHÍZÁS ÉS A PELVIC PADLÓ ZAVARAI AZ IRODALOM ÁTTEKINTÉSE
- A kínai Han lányok SpringerLink elhízással és központi elhízással járó pubertás időzítése
- A reumás ízületi gyulladás fokozott gyulladásos markereivel járó elhízás - A reumatológus
- Az elhízás összefüggésben áll az intersticiális tüdőgyulladás kialakulásával hosszú távú kezelés alatt