4.3 Diszbiózis és depresszió
Bevezetés
Amint azt a korábbi fejezetek tárgyalták, a bél és az agy kétirányú kapcsolata, vagy az bél-agy-tengely, sok kérdést vet fel azzal kapcsolatban, hogy az agy működését hogyan befolyásolja a bél, és fordítva. Pontosabban, a bél mikrobiomjának a mentális betegségekben való részvételének mértékét csak nemrégiben vizsgálták.
Hangulati rendellenességek, mint pl MDD (súlyos depressziós rendellenesség) idiopátiásak és nem végeztek sikeres célzott kezelést, főleg azért, mert sok területet érintenek. E rendellenességek egyik feltételezett célpontja a bél, mivel a mentális betegség és a gyomor-bélrendszeri megbetegedések között magas a komorbiditás aránya. Például sok IBS-ben (irritábilis bél szindróma) szenvedő ember is szenved MDD-ben, az antidepresszánsok az egyetlen gyógyszerek, amelyek sikeresek az IBS kezelésében. Ezért egyértelmű összefüggés van a bél és a mentális betegség között; azt azonban, hogy melyik rendszert érinti először, és ezért melyik egyensúlyhiány vezet a másikhoz, még ki kell deríteni (Rogers et al., 2016).
Ennek a gondnak a megoldására messziről kutatók próbáltak kapcsolatot találni a gyomor-bélrendszeri egyensúlyhiány és az MDD között. Az eddig ismert tény az volt, hogy az MDD számos gasztrointesztinális rendellenességgel jár együtt, és hogy az antidepresszánsok valamilyen módon befolyásolják a bélrendszert, és e rendellenességek kezelésére szolgálnak. Ezért azt javasolták, hogy a bél mikrobiotáját az MDD-nek befolyásolnia kell, ezért az antidepresszánsok, amelyek a legtöbb esetben visszafordítják az állapotot, az MDD által kiváltott bélváltozásokat is visszahozzák a homeosztázisba. Mindezek pusztán sejtések voltak, ezért további vizsgálatoknak kellett utánajárniuk.
Dysbiosis és depresszió
Az első olyan terület, amellyel foglalkozni kellett, az MDD-s betegek bélmikrobiális profiljai és az egészséges kontrollok voltak. Az összehasonlító elemzések olyan technikákkal, mint a 16S rRNS szekvenálása, szignifikáns különbséget mutattak ki a két csoport bélmikrobiális populációi között (lásd 1. ábra). Például egy tanulmány megállapította, hogy az MDD-ben szenvedő betegeknél nagyobb volt a Bacteroidetes relatív bősége és alacsonyabb az Actinobacteriumok relatív bősége az egészséges kontrollokhoz képest (lásd a 4.1. Fejezetet a bakteriális phyláról) (Zheng et al., 2016a). Ezenkívül egy másik tanulmány megállapította, hogy az MDD-ben szenvedő betegeknél magasabb volt az Enterobacteriaceae és az Alistipes szint, de alacsonyabb a Faecalibacterium szintje az egészséges kontrollokhoz képest (Jiang et al., 2015; Liu, 2017). Sőt, egy harmadik tanulmány magasabb Bacteroidales-szintet, de alacsonyabb Lachnospiraceae-szintet állapított meg MDD-s betegeknél az egészséges kontrollokhoz képest (Liu, 2017; Naseribafrouei et al., 2014). Ennélfogva valóban van kapcsolat az MDD patológiája és a bél mikrobiom között, de a kapcsolat iránya nem ismert.
Ennek a komplex kapcsolatnak az irányát igyekeztek megtudni, a kutatók számos módon manipulálták a bél mikrobiómájának összetételét, és megfigyelték a bekövetkezett viselkedési és fiziológiai változásokat, ha voltak ilyenek. A mikrobiom antibiotikumokkal történő teljes kiirtását arra használták fel, hogy felmérjék a bélbaktériumok viselkedésének fontosságát; ez azonban sok vizsgálat alá került, különösen azután, hogy számos tanulmány kimutatta, hogy az antibiotikumoknak óriási hatást fejt ki, sok zavaró tényező bevezetésével. Pontosabban, az antibiotikumok képesek megváltoztatni a mikrobiomot vagy kimerítve, növelve az antibiotikumokkal szemben rezisztens baktériumok számát, vagy közvetlenül befolyásolva a gazdaszövetet. Az antibiotikumok által kiváltott, a gazdaszövetre gyakorolt hatás kiterjedhet a központi idegrendszerre (központi idegrendszerre), potenciálisan neuroaktív hatást fejt ki. Mindezek külön-külön befolyásolhatják a mentális egészséget, és ezért megnehezíthetik az eredmények pusztán a mikrobiotának tulajdonítását (Champagne-Jorgensen et al., 2019; Flux & Lowry, 2020; Morgun et al., 2015).
Pszichobiotikumok
A bél mikrobiomjának gazdagítását olyan szerek segítségével, mint a prebiotikumok és a probiotikumok, szintén széles körben feltárták. Probiotikumok erjesztett élelmiszerekben található élő mikroorganizmusok, amelyek elfogyasztása esetén vélhetően gazdagítják a bél mikrobiomját. A depresszió kezelésére javasolták őket, mivel feltételezhető, hogy javítják a bél egészségét. Annak ellenére, hogy ígéretet tettek terápiás szerként vagy a hagyományos antidepresszánsok kísérőjeként a depresszióban szenvedők tüneteinek enyhítésével, a tanulmányok vegyes eredményeket mutattak, és hatékonyságukról még nem lehet végleges állítást tenni (Flux & Lowry, 2020; Nadeem et al., 2019). Bár a probiotikumokról szóló tanulmányok gyakran olyan személyekre összpontosítottak, akiknek már fennáll a kórképük, az egészséges felnőtteknek adott kiegészítők csak átmeneti hatást gyakoroltak a bél mikrobiomjára. Ennélfogva az univerzális hatás hiánya megkérdőjelezi a hatásmódjukat, és szükségessé teszi, hogy több vizsgálatot végezzenek változatosabb mintákon annak tisztázása érdekében, hogy alkalmazhatók-e a bélet érintő különféle patológiák, például a depresszió kezelésére (Khalesi et al., 2018).
Továbbá, Prebiotikumok olyan anyagok, amelyeket a bél mikrobiota lebonthat, és amelyeknek az embernek nincsenek enzimjei a metabolizmushoz (Flux & Lowry, 2020; Holscher, 2017). Krónikus stressz egereken végzett kísérlet azt mutatta, hogy a prebiotikus adagolás olyan módon befolyásolta az SCFA (rövid láncú zsírsav) szintet, amely korrelál a pozitív viselkedési állapottal. Csökkentette a stresszhormon szintjét, csökkentette a gyulladásgátló citokin szintjét, valamint antidepresszáns és szorongásoldó hatású volt (Burokas et al., 2017; Flux & Lowry, 2020; Kao et al., 2016; Louis et al., 2016). Ezek az eredmények azt mutatják, hogy a prebiotikus kezelés pozitív hatással lehet a depresszióra; a probiotikumokhoz hasonlóan azonban további vizsgálatokat is el kell végezni annak érdekében, hogy határozottan állítsák hatékonyságát.
A prebiotikumok és a probiotikumok kombinálhatók a modernebb kifejezés alatt „Pszichobiotikumok” amelyet a közelmúltban hoztak létre, hogy utaljon minden olyan bakteriális szerre, amely befolyásolja a mentális egészséget. Azonban gyakran vegyes eredmények vannak arról, hogy ezek a tápanyagok hogyan befolyásolják a mentális egészséget és viselkedést. Ezért ennek a gondolatnak a tisztázása érdekében további vizsgálatokat kell végezni nagyobb minták felhasználásával és több emberi kísérlettel (Flux & Lowry, 2020; Sarkar et al., 2016).
Mikrobiota transzfer
Egy másik technika, amelyet a dysbiosis és a depresszió kapcsolatának tanulmányozására használtak, az FMT (Fecal Microbiota Transfer). Ebben a technikában a székletmintákat kivonják egy donortól, és különböző formákban adják be a befogadónak. A bélmikrobiómák kutatásában az FMT-t úgy hajtják végre, hogy az emberi ürülékmintákat GF (Germ-Free) vagy SPF (Specific Pathogen Free) egerekbe helyezik a betegségmodellek létrehozása érdekében. Számos tanulmány használta ezt a technikát a különféle rendellenességek, köztük az MDD bélrendszeri hatásainak vizsgálatára. Egy tanulmányban székletmintákat gyűjtöttek MDD-s betegekből vagy egészséges kontrollokból, és egészséges GF egereknek adták be. Az eredmények azt mutatták, hogy az MDD-ből származó mikrobiotát kapó egerek depressziószerű viselkedést mutattak, például a mozgásszervi teszteknél hosszabb mozdulatlanságot, valamint az MDD patológia egyéb viselkedési és fiziológiai tünetei között az anyagcsere-aktivitás zavarait (Zheng et al., 2016b). Ez azt mutatja, hogy a mikrobiota transzfer önmagában depressziót indukálhat az egyébként egészséges egerekben.
Mivel az FMT kimutatták, hogy depressziót vált ki, felmerül a kérdés, hogy alkalmazható-e az állapot megfordítására. Ha ez a technika hatékony a bél mikrobiota összetételének megváltoztatásában, akkor a depresszió által kiváltott dysbiosist egészséges mikrobiota transzferrel kell csillapítani; ezt azonban még nem tesztelték. Sőt, bár az FMT-t számos patológia lehetséges kezelésének tekintik, például az ASD-t (autizmus-spektrum-rendellenesség), még mindig gyerekcipőben jár, és emberben még nem tesztelték széles körben (Kang et al., 2017). Emellett az emberi bél mikrobiomjának természetes változása megnehezíti a transzplantációra használandó egészséges mikrobiota egyedi mintájának standardizálását (Flux & Lowry, 2020; Human Microbiome Project Consortium, 2012). Ennélfogva még kérdéses, hogy az FMT alkalmazható-e az MDD és más ilyen állapotok lehetséges kezelésében, és hogy életképes-e és általánosítható-e az emberek számára.
Sokoldalú rendellenesség
A bél-agy tengelyhez hasonlóan hasonló autópálya néven ismert mikrobiom-bél-agy-tengely úgy gondolják, hogy a mikrobiota és a központi idegrendszer közötti kétirányú kommunikációs forma, amely végső soron befolyásolja a viselkedést. Bár a fent vázolt kutatás nagyon szoros kapcsolatot mutat a depresszió és a dysbiosis között, az egyensúlyhiányok végleges sorrendjét nehéz elkülönítve megérteni. Ehelyett a bélmikrobiom és a depresszió kölcsönhatását kétirányú kommunikációnak kell tekinteni, amely számos más rendszertől és tényezőtől függ. Ennélfogva a bél mikrobioma közvetlenül befolyásolhatja a központi idegrendszert metabolitjai, például SCFA-k és a vagus idegen keresztül haladó citokinek, vagy közvetett módon az enterális rendszer útján. Ezzel szemben a központi idegrendszer olyan faktorokat szabadíthat fel, amelyek befolyásolják a bél, a bél permeabilitását és a mikrobiota összetételét (lásd 2. és 3. ábra). Ez a teljes rendszer, valamint a két komponens, a bél mikrobioma és az agy közötti kommunikáció lehetővé teszi a depresszió árnyalt megnyilvánulását, amelyet értelmesen nem lehet megérteni, hacsak átfogó kitekintést nem alkalmazunk (Flux & Lowry, 2020).
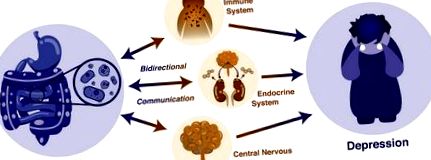
3. ábra. A depresszió több fiziológiai tényezőre gyakorolt hatása és ezek együttes hatása a bél- és a mentális egészségre. Adaptálva: „A bélrendszer megtalálása: A mikrobiom integrálása a depressziós mechanizmusok holisztikus nézetébe”, a kezelés és az ellenálló képesség témaköréből. Flux, M. C., & Lowry, C. 2020, Neurobiology of Disease, 135 (104578).
Kihívó kérdések
1. Tervezzen meg egy kísérletet a mikrobiom-bél-agy tengely irányultságának és depresszióra gyakorolt hatásának vizsgálatára.
2. Hogyan lehet felhasználni a bél mikrobiómáját a depresszió lehetséges kezelésében, és milyen figyelmeztetések vannak a bélrel kapcsolatos, fentebb javasolt kezelésekre?
3. Hogyan lehet hatékonyan kezelni a bélben a depresszió által okozott egyensúlyhiányt a már meglévő kezelési technikákban?
Kulcsszavak
Bél-agy tengely; MDD; Probiotikumok; Prebiotikumok; Pszichobiotikumok; FMT; Mikrobiom-bél-agy-tengely
- Tippek a depresszió kezeléséhez - NHS
- Az étel, a szorongás és a depresszió mögött álló pszichológia A sportdoktor kréta beszélgetése dr
- Depresszió
- A kóros elhízás leverő depressziója - VICE
- A tesztoszteron egyensúlyhiány összekapcsolhatja a depressziót és a megnövekedett testtömeget a premenopauzás nőknél