Savasodás
A GDL vagy a citromsav által kiváltott savasodást csökkentett hőmérsékleten sem lehet megállítani, mivel ez kémiai folyamat, és amíg rendelkezésre áll szabad víz és GDL, a GDL glükonsavvá alakul át, függetlenül attól, hogy milyen hőmérsékleten zajlik a reakció.
Kapcsolódó kifejezések:
- Kovász
- Joghurt
- Erjesztett tej
- Kappa-kazein
- Sajtkészítés
- Ütő
- Szalámi
- Kazein
- Kezdő kultúra
Letöltés PDF formátumban
Erről az oldalról
Tejipari alapú funkcionális italok
Deepak Mudgil, Sheweta Barak, Tej alapú italok, 2019
3.3.1.2. Savasság
A gyümölcslevek mikrobiális fertőtlenítése
Savasodás
A savasodást a nemkívánatos mikroorganizmusok, ezen belül a kórokozók szaporodásának szabályozásának eszközeként ismerik el. Az erjesztést, a természetben előforduló savanyítás egyik formáját régóta használják az élelmiszerek tartósításához, csakúgy, mint a szerves és egyéb megfelelő savak közvetlen hozzáadásával történő savanyítást (Brown és Booth, 1991). A savanyító szereket, például a citromsavat és az almasavat, általában a léitalokban és gyümölcstermékekben használják pH-beállításhoz és ízesítéshez (Somogyi, 2005). Míg a savanyítást ritkán alkalmazzák a gyümölcslében levő kórokozó szervezetek egyedüli ellenőrzési mechanizmusaként, kontroll lépésként a pasztörizált és túlélő C. botulinum spórákkal szennyezett pasztőrözött, hűtött alacsonyabb savtartalmú gyümölcslevek, például sárgarépa előállítására ajánlották. később növekedhet, ha a fogyasztói csomagot hőmérséklet-visszaélésnek vetik alá (US FDA, 2007). Ezt az útmutatót a hűtött sárgarépaléhez kapcsolódó botulizmus kitörésére adott válaszként adták ki 2006-ban.
Sajttej készítése
P.L.H. McSweeney,. T.P. Guinee, a megoldott sajtproblémákban, 2007
pH-ciklus
A felhevített tej savanyítása kb. A pH 5,5, majd 20 ° C-on tartás és pH 6,6-ig történő semlegesítés csökkenti a felmelegített tej RCT-értékét és kissé szilárdabb géleket eredményez. A savanyítás a kolloid kalcium-foszfátot oldja fel [4], amely semlegesítéskor újrareccsen, de a fűtetlen tejhez közelebb álló formában. Egyes munkavállalók azt tapasztalták, hogy a tej pH-jának 7,3-ra történő beállítása a pH-ciklus előtt tovább javítja a tej oltóalvadási tulajdonságait. Összességében a pH-ciklus nagyobb hatással van a melegített tej RCT-értékének javítására, mint a gél szilárdságára.
Savval alvadt tejgélek kialakulása, szerkezeti tulajdonságai és reológiája
Az összetétel és a feldolgozás paramétereinek hatása a savas tejgélek texturális tulajdonságaira
Az egyes feldolgozási lépések hatásait a savas tejgélek texturális tulajdonságaira a következő szakaszban vesszük figyelembe. Néhány fő feldolgozási tényező hatásainak összefoglalását a 7.3. Táblázat tartalmazza .
7.3. Táblázat Összefoglalás egyes feldolgozási körülmények hatásáról a tej savas koagulálására és az eredményezett gél tulajdonságaira
| Inkubációs hőmérséklet | A gyorsabb savtermelés magasabb hőmérsékleten rövidebb gélesedési időkhöz vezet. Magasabb hőmérsékleten (pl. 30 ° C) több kazein részecske átrendeződése van a hálózatban, ami alacsonyabb platóértékeket ad a gélmerevséghez és megnövekszik a tejsavó-elválasztás valószínűsége, mint az alacsonyabb hőmérsékleten (pl. 23 ° C) készített gélek . Nagyon magas hőmérsékleten a gélesedési pH növekedhet. Nagyon alacsony hőmérsékleten (például 4 ° C) a 4,6-os pH mellett sem következik be kazein alvadása. |
| Hőkezelés | A tej hőkezelése ≥78 ° C hőmérsékleten ≥5 percig elegendő tejsavófehérje-denaturációt eredményez a gélesedés pH-jának jelentős növeléséhez, a gélesedési idő csökkentéséhez és a viszkozitás/szilárdság növeléséhez. A fő tejsavófehérje, a β-laktoglobulin magas izoelektromos pontja (5,3) felelős ezért. A kazeinszálak diszulfid keresztkötése növeli a gél merevségét, de a CCP szolubilizációja már a gélmátrixban részt vevő kazein részecskéknél bekövetkezik, ami nagyobb átrendeződéseket vált ki és felelős a reológiai vizsgálatokban megfigyelt veszteség tangens növekedéséért. |
| pH | Az aggregáció a kazein izoelektromos pontjának (≤4,9) megközelítésével történik. A maximális gélkeménység pH 4,6 körül alakul ki. Általában a lassabb savasodás sebessége kissé nagyobb gél szilárdságot eredményez. |
| Ionikus erő | Nagyon nagy ionerősség mellett (például 0,1 M NaCl) az elektrosztatikus töltetek szűrése miatt a kazein részecskék nem aggregálódnak 4,6-os pH-n. A savas koagulációhoz minimális Ca 2+ koncentráció szükséges. |
| Kazeintartalom | A gélmerevség arányos a kazein koncentrációjával |
| Oltó használata | Nagyon kis mennyiségű oltó használata néhány friss típusú sajtban azt eredményezi, hogy a gélesedés korábban (azaz magasabb pH-nál) bekövetkezik, és nagyobb a szinerézis a feldolgozás során (pl. Főzés). |
Oltás, gélesedési hőmérséklet és savanyítási módszer
A friss savtermékek tenyészetek általi megsavanyítását általában két módszer bármelyikével végezzük: lassú, 12–16 óra 20–23 ° C-on (hosszú kötés) vagy 4–6 óra 30–32 ° C-on (rövid beállított időtartam). Mezofil tejsavbaktériumok (azaz főként Lactococcus spp. És Leuconstoc spp.) Tenyészeteit és néha probiotikus fajokat használnak tenyészeteként a legtöbb savval koagulált sajt számára. Néha a friss sajtok sav hozzáadásával készülnek, például foszforsav vagy tejsav (közvetlen savmegkötés vagy közvetlen savanyítás) és/vagy GDL.
A 20 ° C-on készített gélekkel összehasonlítva a 40 ° C-on készített savas kazein gélek durvábbak, több átrendeződést mutatnak, gyengébbek és kevésbé stabilak (Lucey és mtsai, 1997c, d). A gyakorlatban más folyamatváltozók (például zsírtartalom, stabilizátorok, hőkezelés) segíthetnek az ilyen típusú gél stabilizálásában. Általánosságban elmondható, hogy a magas inkubációs hőmérsékleten (pl. 45 ° C) a savfejlődés túlzott üteme (pl. GDL alkalmazása) hozzájárul a „wheying off” hibához és a gyenge gélképződéshez. A fermentációs idő jelentősen befolyásolja a CCP szolubilizációs sebességét. A hosszú fermentációs idők (lassú savasodás) több időt engednek a CCP oldódására (magasabb oldható Ca-tartalom a gélekben), míg a rövid fermentációs idők (gyors savasodás) kevesebb időt engednek ennek a folyamatnak a megvalósulásához (alacsonyabb oldható Ca-tartalom gélekben) (Peng et al., 2009).
Különböző típusú tenyészetekkel vagy GDL-lel képzett savas tejgélekben az alacsonyabb gélesedési hőmérséklet (pl. 30 ° C) hosszabb gélesedési időt eredményez, de ezeknek a géleknek magasabb a G'-értéke, mint a sokkal magasabb gélesedési hőmérsékleten készített géleknek (pl. (40 ° C) (Cobos és mtsai, 1995; Lee és Lucey, 2004; Lucey és mtsai, 1998d). Ennek oka a durvább gélszerkezet (nagyobb átrendeződések) a magas hőmérsékleten képződő gélekben (Lucey és mtsai, 1997d). A savas gélek dinamikus modulusai a mérési hőmérséklet csökkenésével nőnek (Lucey és mtsai, 1997b, c). Az alacsonyabb gélesedési hőmérsékleten készített savtej zselékben csökken a savó szétválasztása és a gél permeabilitása (Lee és Lucey, 2004; Lucey és mtsai, 1997d, 1998a). Peng és mtsai. (2010) a hőmérséklet megváltoztatásának hatását vizsgálta közvetlenül a savas tejgél képződése után. A gélesedés utáni lehűlés a gél merevségének növekedését és az interlusterek közötti szálképződés fokozódását eredményezte, míg a gélek felmelegedése elősegítheti a klaszterek közötti fúziót és a szálak törését.
A sav által indukált tejgélek úgy képződhetnek, hogy a tejet savval (pl. HCl) lassan megsavanyítják alacsony hőmérsékleten (például Roefs, 1986). A 4,6-hoz közeli pH-értékű kazeinrészecskék nagyon eltérnek a normál, fiziológiai pH-értéktől (Walstra, 1993).
Hammelehle és mtsai. (1997, 1998) citromsavat használtak savas tejgélek előállítására ezzel a hideg savasítási eljárással. Megállapították, hogy az izoelektromos pont közelében nehezebb homogén gélt kapni, amikor a mintákat később felmelegítették. A gélek alacsonyabb melegítési hőmérsékleten képződtek, amikor a savanyítási pH alacsonyabb volt. Magasabb kötési hőmérséklet (például 40 ° C a 30 ° C-hoz képest) szilárdabb géleket eredményezett, ami ellentétes tendencia a GDL gélekkel szemben. Valószínű, hogy a GDL és a közvetlenül savasított savas tejgélek szerkezete eltér. A savasítás és a gélképzés módszere (pl. GDL, hideg savanyítás vagy bakteriális fermentáció) nagy hatással van a savas tejgélek szerkezetére és fizikai tulajdonságaira (Lucey és mtsai, 1998d; Roefs, 1986). A hideg, savanyított gélek gyors, nagyon magas hőmérsékletre (pl. 50 ° C) történő melegítése szilárd géleket eredményezett, de jelentős szinézist eredményezett.
A tejet reverzibilisen megsavanyítják karbonizálással, a savas pH-érték csökkentése céljából (általában alacsony hőmérsékleten végezzük) a nyomás alá helyezett CO2-t injektálva savanyító szerként. A semlegesítést nyomásfelszabadítással, majd vákuumban végzett gázmentesítéssel érhetjük el. A CO2-kezelt tejből származó (GDL felhasználásával készült) savgélek reológiai tulajdonságai hasonlóak voltak a kezeletlen tejből származó savgélekéihez (Raouche és mtsai, 2007).
A tej alapú élelmiszerek felépítésének alapjai
A micelláris szerkezet módosítása savanyítással
A tej savanyítása nemcsak a joghurtgyártásban, hanem a sajt különféle fajtáinak előállításában is fontos. A micellák számos szerkezeti tényezője megváltozik a tej savasodásával. Először, és ami talán a legfontosabb, a micellás CCP fokozatosan oldódik, mivel a pH csökken a tej természetes pH-jához (~ 6,7) képest (Dalgleish és Law, 1989; Le Graët és Gaucheron, 1999). Tejsavas baktériumok vagy kis mennyiségű GDL alkalmazásával történő lassú savanyítással a Ca és Pi felszabadulása a micellákból pszeudo-egyensúlyi folyamat (Law és Leaver, 1998; Dalgleish és mtsai, 2005). A CCP eltávolítása kb. 5,1 pH-értékkel befejeződik.
A savasodás a szőrös felületi réteg összeomlását okozza. Semleges pH-nál ez a réteg fel van töltve, és a töltés taszításai fenntartják a hajszálakat. Mivel a pH csökkenése során a töltések csökkennek, a hajszálak kevésbé nyúlnak ki, ezért kevésbé stabilizálódnak (de Kruif, 1997). A szőrös réteg ilyen összeomlását a részecskék hidrodinamikai sugarának csökkenése a savasodás során sugallja (Alexander és Dalgleish, 2005). Végül körülbelül 5,0 pH mellett a szőrszálak teljesen összeomlanak, a szterikus stabilizáció minimálisra csökken, és a fehérjék töltése a minimumon van. A bezáráshoz vezető energiagátló alacsony, és a micellák ezután aggregálódhatnak. Feltételezzük, hogy a szőrös réteg összeomlása homogén lenne a micelláris felületen, így reaktív „forró pontok” nem jönnek létre.
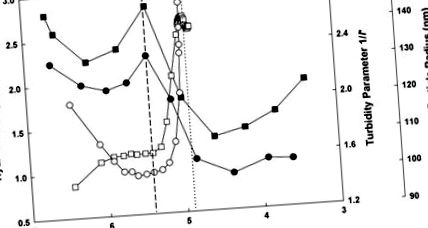
3.2. ÁBRA A kazein micellák változásai a savasodás során. Snoeren és mtsai hidratálási eredményei (kitöltött négyzetek). (1984) és Ahmad és mtsai (kitöltött körök). (2008), a részecskesugár (nyitott körök) és az 1/l tur (nyitott négyzetek) zavarossági paraméter változásával együtt, diffúz hullámspektroszkópiával mérve (Alexander és Dalgleish, 2005). A szaggatott vonal azt a pH-t jelöli, ahol kiterjedt gélesedés történik, a szakadt vonal pedig a hidratáció, a részecskeméret és az optikai tulajdonságok változásának megfelelőségét mutatja.
A megsavanyított micellák aggregációja izoelektromos pontjuk közelében összekapcsolt részecskék háromdimenziós hálózatának létrejöttéhez vezet (3.3. Ábra), és a részecskék nem veszítik el identitásukat (vagyis a micellák nem olvadnak össze). Ez a gélszerkezet a diffúzióval korlátozott klaszter – klaszter kölcsönhatás eredménye, amely egy fraktál típusú aggregátumot eredményez: vagyis nincs különösebb irányultság a gélszerkezet kialakulásában. Másrészt, mivel a gél meglehetősen gyorsan képződik és kinetikus szabályozás alatt van, az aggregátumok nincsenek az optimális szabadenergia-konfigurációban. Különösen azért, mert a gélben levő micellás részecskéket kovalens kötések nem tartják össze, lehetséges, hogy a gélen belül mozogjanak. Így a gél belső struktúrájának megváltozásával szinerézisen megy keresztül, a víz kiszorításával, mivel az alkotó micellák szorosan érintkeznek és szorosabb mátrixot képeznek.
3.3. ÁBRA (A) fűtetlen és (B) fűtött tejből származó savgélek szerkezete. A mikrográfiák a micella különböző típusú érintkezéseit mutatják be a két esetben. Az (A) pontban a micellák megkülönböztethetőek maradnak a gélen belül, és a (B) pontban a hozzájuk kapcsolódó tejsavófehérje vonja össze őket, és szálakat képez közöttük. Az (A) skála 1 μm, (B) 500 nm.
- Atherogén étrend - áttekintés a ScienceDirect témákról
- Akut hasnyálmirigy-gyulladás - áttekintés a ScienceDirect témákról
- Akut gégegyulladás - áttekintés a ScienceDirect témákról
- Atrófiás gyomorhurut - áttekintés a ScienceDirect témákról
- Autoimmun pajzsmirigy-gyulladás - áttekintés a ScienceDirect témákról