Magányos plazmacytoma csont keresztcsont felett: esettanulmány
Hszin-Lin Csen 1, Jing-Hsziang Csu 1,2, Yueh-Csun Lee 1, Hszen-Csun Tseng 1,3
Absztrakt: A magányos csont plazmacytoma (SPB), más néven csontos plazmacytoma, gyakrabban fordul elő férfiaknál, mint nőknél, becsült arányuk 2: 1. Az SPB-betegek medián életkora körülbelül 55 év. A lokalizált sugárterápia az első vonalbeli kezelés a mielóma multiplex kialakulásának elkerülése érdekében. Egy 46 éves férfi 3 hónapig az alsó végtagjaiba sugárzó alsó hátfájás miatt látogatott kórházunkba. Az L-gerinces MRI S2-S4 csonteróziót mutatott a keresztcsont felett egy nagy (8,8 × 6,2 cm) daganattal. A tumor részleges eltávolítását követően a patológia plazmacitómát mutatott. Adjuváns sugárterápiát 50 Gy-vel 25 frakcióban adtunk a bruttó tumornak volumetrikus modulált ívterápia (VMAT) alapján. Adjuváns kemoterápiát nem végeztek. A medence CT-t 3 havonta rendezték a 24 hónapos követés során. A követési periódus alatt nem volt távoli áttét vagy újonnan diagnosztizált myeloma multiplex.
Kulcsszavak: Plasmacytoma; csontdaganat; sugárkezelés
Beérkezett: 2018. november 18 .; Elfogadva: 2019. február 25 .; Publikálva: 2019. március 12.
Bevezetés
A plazmasejtek rosszindulatú daganatai a rákcsoportok, amelyek a plazma sejtekből szaporodtak. Ezeket a rákokat egyszeri vagy többszörös elváltozásokba sorolhatjuk. Az előbbi magányos plazmacytoma, míg az utóbbi myeloma multiplex. A magányos plazmacitómák előfordulhatnak a csontban vagy a lágy szövetekben, és nagy a kockázata a mielóma multiplexbe történő progressziónak. Itt egy olyan beteget tekintettünk át, akinek a keresztcsont felett egyedüli csont plazmacytoma (SPB) volt, sugárkezelésen esett át.
Eset bemutatása
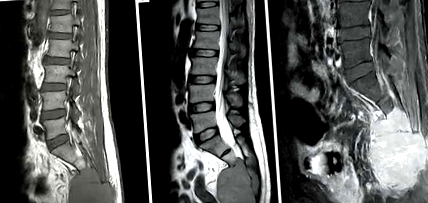
Egy 46 éves férfi 3 hónapig járt a kórházunkban az alsó hátfájás miatt. Korábbi kórtörténete csak a magas vérnyomást tartalmazta trauma nélkül. Az alsó végtagokig sugárzó fájdalmat zsibbadás kísérte. A fájdalom súlyosbító tényezői a hosszan tartó álló és ülő helyzetek voltak. A szakaszos claudicálás miatt hosszú ideig nem tudta elviselni az ambíciót. 3 kg alatt körülbelül 12 kg testtömeg-csökkenést is megállapítottak. Nem volt vizelet vagy széklet inkontinencia. Az L-gerinc és a kismedencei mágneses rezonancia képalkotást (MRI) rendezték, és a keresztcsont felett egy nagy daganatot (8,8 cm × 6,2 cm) tártak fel. A medence feletti foglaltsági elváltozás a keresztcsontot érintette (S2-S4), hipointenzitással mind a T1-súlyozott, mind a T2-súlyozott képeken. Homogén kontrasztjavító hatású volt (1A, B, C ábra). Ezután 2016. május 31-én műtéti beavatkozást kapott részleges daganateltávolítással. A patológiai jelentés kimutatta a keresztcsont és a lágyrész plazmacitómáját. A lágyrészben csontos invázióval diffúz plazmacitoid sejteket találtunk excentrikus magokkal. Az immunhisztokémiai vizsgálat kimutatta, hogy a tumorsejtek citokeratinokat (CK) (-), Differenciálódási klasztert (CD) 138 (+), Kappa könnyű láncot (-), Lambda könnyű láncot (+) és CD 20 (-) mutatnak be (2-4. Ábra). ). A β2 mikroglobulin a tumor kivágása után 3270 nanogramm/milliliter volt.
Az SPB diagnózisa alatt részleges tumoreltávolítást és adjuváns sugárterápiát rendeztek. A számítógépes tomográfia (CT) -szimulációt 2016. június 13-án végeztük. CT-szimulátorral 5 mm-es szelet kontraszterősítésű CT-képek sorozatát készítettük. A CT-képeket átvittük a tervezési rendszerbe a célmeghatározás céljából. A beállítási hiba elszámolásához a tervezési céltérfogat (PTV) 5 milliméteres tartalékot tartalmazott a klinikai céltérfogat (CTV) körül. Hat megavoltos (MV) fotont használtak volumetrikus modulált ívterápiás (VMAT) technikával. Az előírt adag 50 szürke (Gy) volt napi 2 Gy frakcióban a PTV-re. A kezelést hetente 5 napon keresztül, összesen 25 frakcióban végeztük. A VMAT-t úgy optimalizálták, hogy a PTV 100% -át lefedje az előírt dózis 100% -ával. A végbél dóziskorlátozása miatt a rektális dózist 45 Gy értékre állították be, ami 12% -kal kevesebb volt, mint 50 Gy. A sugárkezelést a műtét utáni 20. napon (2016. június 20. és 2016. július 22. között) kezdték meg (5,6. Ábra). A kezelés után a betegnek nem volt akut reakciója. Sem dermatitist, sem emésztőrendszeri kényelmetlenséget nem figyeltek meg.
Onkológushoz fordultak, és a csontvelő biopsziát javasolták a myeloma multiplex kizárására. A csontvelő biopszia hipocellularitást (20–30%) mutatott a csontvelőben és a szétszórt plazma sejtekben (
Vita
Az SPB-t csontos plazmacitómának is nevezik. Ez a magányos plazmacytoma egyik típusa. Az SPB leginkább axiális csontvázban, csigolyatestekben és a koponyában fordul elő (1,2). Az SPB-k gyakrabban fordulnak elő férfiaknál, és a férfi-nő arány körülbelül 2: 1. Az SPB-ben szenvedő betegek medián életkora 55 év körüli, ami körülbelül 10 évvel alacsonyabb, mint a mielóma multiplexben szenvedőké (3). Az SPB előfordulása körülbelül 3,5/1 millió (4). Az irodalom áttekintése az SPB előfordulását mutatja be a különböző etnikai csoportok számára. Az ázsiai lakosságra vonatkozó adatok azonban hiányoznak. Csak a tajvani vizsgálatok szerint az SPB előfordulása az összes plazma neoplazma között 6,2% (1). Az M-fehérjéről, amely egy monoklonális paraprotein, rossz prognosztikai tényezőt találtak, ha egy évnél hosszabb ideig létezett, és 2,2 éven belül kezeléssel vagy anélkül kezeléssel társult a myeloma multiplex kialakulásához (5).
Az SPB diagnózisához biopsziával igazolt magányos csonttumor szükséges, klónikus plazmasejtek bizonyítékával a csont egyetlen területén és az MRI gerincének további elváltozásai nélkül. A kóros immunhisztokémiai vizsgálat CD 138 és lambda könnyű lánc pozitív lehet. Nem lehet bizonyíték a szisztémás mielómára, mint például vérszegénység, hiperkalcémia vagy vesefunkció-károsodás (6). Ezenkívül a csontvelő aspirátumban, a szérumban vagy a vizeletben nem szabad monoklonális plazmasejteket tartalmazni (3).
Képalkotó jelentések szerint az SPB többnyire a csigolyákban és a hosszú csontokban található (7). A kezelés előtt az SPB elváltozások gyakran homogén alacsony jelintenzitást mutatnak a T1-súlyozott képeken, és nagy jelintenzitást mutatnak a T2-súlyozott képeken. Az MRI a tömeg növelése szempontjából előnyösebb, mint a CT. Az MRI markáns homogén fokozása hasznos lehet a kismedencei SPB diagnózisában (8). Esetünkben a kismedencei MRI elváltozás hipointenzív volt mind a T1, mind a T2 súlyozott képeken, és homogén kontraszterősítésű volt. A kismedencei tömeg nagy jelintenzitást mutatott a rövid tau inverzió helyreállítási szakaszában.
Az SPB-nek nagy a kockázata a mielóma multiplex kialakulásának. Az elsődleges kezelés lokalizált sugárterápia ennek a progressziónak az elkerülése érdekében, amely az esetek 50% -ában 5 éven belül, 65-84% -ban 10 év alatt, 65-100% -ban 15 év alatt következik be (4,6). Az SPB optimális terápiájának a hosszú távú lokális kontroll elérésére kell törekednie, a mielóma multiplex minimális morbiditásával. A végleges helyi sugárkezelés mesés helyi kontrollt biztosíthat, tartós remisszióvá válhat, sőt gyógyulást is eredményezhet. Esetünkben továbbra is hosszú távú, 5-10 évig tartó nyomon követésre van szükség.
A sugárterápia kimutatta, hogy kiváló helyi kontrollt biztosít az SPB-k felett. A legnagyobb retrospektív vizsgálatban (n = 258) SPB-ben (n = 206) vagy extramedulláris plazmacytomában (n = 52) szenvedő betegek vettek részt (10). A kezelések magukban foglalták a sugárterápiát egyedül (n = 214), a sugárterápiát plusz kemoterápiát (n = 34) és a műtétet egyedül (n = 8). Az ötéves teljes túlélés 74%, a betegségtől mentes túlélés 50%, a helyi kontroll pedig 85% volt. A lokalizált sugárterápiában részesülő betegeknél kisebb volt a helyi kiújulás aránya (12%), mint azoknál, akik nem részesültek sugárterápiában.
Számos retrospektív vizsgálat csak kisszámú beteget vont be, az SPB alacsony prevalenciája miatt (6) (1. táblázat). A szokásos kezelés a végleges helyi sugárterápia. A kezelési területen az MRI használata ajánlott a GTV meghatározásához. Az MRI erősségei a magas lágyrész kontraszt és a multiplanáris képalkotás. CT-vizsgálatot is kell végezni a csont rendellenességének kimutatására. Így a kezelési teret mind a CT kép, mind az MRI összehasonlításával kell meghatározni. A tervezés kezelésének területe azonban továbbra is ellentmondásos. Egyes szerzők azt javasolták, hogy egész csontot vegyenek be a sugárzási mezőbe a marginális megismétlődés elkerülése érdekében, míg mások azt javasolják, hogy csak a csont egy részét vegyék fel. A CTV esetében legalább 1,5–2 cm margót öleltünk fel az MRI-n, a PTV esetében pedig 5–10 mm margót. Egyes szerzők 40–50 Gy dózist javasoltak kisebb elváltozások esetén (50 Gy nagyobb elváltozások esetén (> 5 cm) (2,3). Suh és mtsai. Javasolt 5 cm-es dózisok) (16). Egy multicentrikus Ritka Rák Hálózat vizsgálatban 258 csontos (n = 206) és extramedulláris (n = 52) SPB-s beteget kezeltek a Princess Margaret Kórházban. Nem találtak dózis-válasz összefüggést a> 30 Gy dózisok esetén, még nagyobb daganatok esetében sem (10). Esetünkben 50 Gy dózist választottunk 25 frakcióban a nagy daganatméret (8,8 cm × 6,2 cm) miatt.
Az adjuváns kemoterápia alkalmazása ellentmondásos. Bizonyos vizsgálatokban az adjuváns kemoterápia nem mutatott semmilyen előnyt a betegség kontrollja vagy a myeloma multiplex progressziójának megakadályozása szempontjából (1,6). Egy prospektív vizsgálatban kimutatták a helyi sugárterápiával végzett kombinált kezelés előnyeit 40-50 Gy (28 beteg) dózisokkal, majd 6 hétente melfalánnal és prednizonnal 3 éven át, csak a radioterápiával (25 beteg) szemben (17). A medián 8,9 éves követés után a betegségmentes túlélés és a teljes túlélés javult a kombinált terápiával kezelt betegeknél. Ezenkívül 22 beteg maradt életben és betegségektől mentesen a kombinált kezelési csoportban, szemben a csak sugárterápiás csoportban csak 13 beteggel (P
Köszönetnyilvánítás
Lábjegyzet
Érdekkonfliktusok: A szerzőknek nem jelentenek be összeférhetetlenséget.
Tájékoztatott beleegyezés: A betegtől írásos tájékoztatáson alapuló beleegyezést szereztek a kézirat és a hozzá tartozó képek közzétételéhez.
- Súlyos súlygyarapodás hosszú hatású injekciós riszperidonnal Esettanulmány
- Jelentős súlycsökkenés a klozapin használatát követően, hogyan lehetséges Ez esetleírás és áttekintése
- A stroke, mint a multile méhek nagyon ritka szövődménye az esetjelentés Iris Publishers
- Scorbut ernyedten és gyengén mutatja be az esetjelentést BMC Pediatrics Teljes szöveg
- Netflix; A To The The Bone elakadt a múltban, amikor a test problémáival kapcsolatos beszélgetésekről volt szó - MOST