Gyulladás és inzulinrezisztencia jellemzése magas zsírtartalmú étrend okozta hím C57BL/6J elhízás modellben
Lenox Hill Kórház, Friedman Diabetes Intézet, Northwell Health, New York, NY, USA
A Feinstein Orvosi Kutatóintézetek, Northwell Health, Manhasset, NY, USA
Donald és Barbara Zucker Orvostudományi Kar, Hofstra/Northwell, Hempstead, NY, USA
Levelezés
Dimiter Avtanski, Ph.D., Friedman Diabetes Institute, Northwell Health, 110 E 59th Street, Suite 8B, 837-es szoba, New York, NY 10022, USA.
A Feinstein Orvosi Kutatóintézetek, Northwell Health, Manhasset, NY, USA
Donald és Barbara Zucker Orvostudományi Kar, Hofstra/Northwell, Hempstead, NY, USA
A Feinstein Orvosi Kutatóintézetek, Northwell Health, Manhasset, NY, USA
Donald és Barbara Zucker Orvostudományi Kar, Hofstra/Northwell, Hempstead, NY, USA
Lenox Hill Kórház, Friedman Diabetes Intézet, Northwell Health, New York, NY, USA
A Feinstein Orvosi Kutatóintézetek, Northwell Health, Manhasset, NY, USA
Donald és Barbara Zucker Orvostudományi Kar, Hofstra/Northwell, Hempstead, NY, USA
Lenox Hill Kórház, Friedman Diabetes Intézet, Northwell Health, New York, NY, USA
A Feinstein Orvosi Kutatóintézetek, Northwell Health, Manhasset, NY, USA
Donald és Barbara Zucker Orvostudományi Kar, Hofstra/Northwell, Hempstead, NY, USA
Levelezés
Dimiter Avtanski, Ph.D., Friedman Diabetes Institute, Northwell Health, 110 E 59th Street, Suite 8B, 837-es szoba, New York, NY 10022, USA.
A Feinstein Orvosi Kutatóintézetek, Northwell Health, Manhasset, NY, USA
Donald és Barbara Zucker Orvostudományi Kar, Hofstra/Northwell, Hempstead, NY, USA
A Feinstein Orvosi Kutatóintézetek, Northwell Health, Manhasset, NY, USA
Donald és Barbara Zucker Orvostudományi Kar, Hofstra/Northwell, Hempstead, NY, USA
Lenox Hill Kórház, Friedman Diabetes Intézet, Northwell Health, New York, NY, USA
A Feinstein Orvosi Kutatóintézetek, Northwell Health, Manhasset, NY, USA
Donald és Barbara Zucker Orvostudományi Kar, Hofstra/Northwell, Hempstead, NY, USA
Absztrakt
Háttér
Az étrend okozta elhízás (DIO) állatmodelljeit általában használják az orvosi kutatások során az emberi betegségek utánzására. Nincs univerzális állatmodell, és az új kísérletek megtervezésekor figyelembe kell venni a különféle tényezők gondos értékelését. Itt megvizsgáltuk a 9 hetes, magas zsírtartalmú étrend (HFD) 60% -os zsíros energiát biztosító beavatkozásának hatását a gyulladás és az inzulinrezisztencia paramétereire hím C57BL/6J egerekben.
Mód
Hat hetes egereket kezdtek el rendszeres táplálékkal (RD) vagy HFD-vel, 60 hét kcal energiát adva zsírból 9 hétig. Az éhomi vércukorszintet glükométerrel, az inzulin és az előgyulladásos citokinek éhomi plazmaszintjét Luminex-vizsgálattal mértük. Az inzulinérzékenységet QUICKI és HOMA2 indexek alkalmazásával értékeltük.
Eredmények
HFD egerek mutatták
40% -kal nagyobb testtömeg és
20% -kal nagyobb hasi kerület, a fehér zsírszövet tömegének növekedése miatt. A májvizsgálat a HFD egerek májában megnövekedett méretet és magasabb máj lipidfelhalmozódást mutatott ki RD társaikhoz képest. A HFD csoportba tartozó állatokat szignifikánsan magasabb korona-szerű struktúrák (CLS) jelenléte jellemezte a WAT-ban és magasabb proinflammatorikus citokinek (TNF-α, IL-6, leptin, MCP-1, PAI-1 és rezisztin) plazmaszintje volt. . A HFD-vel táplált egerek szintén csökkent inzulinérzékenységet mutatnak (alacsonyabb QUICKI, magasabb HOMA-inzulinrezisztencia (HOMA-IR) és alacsonyabb HOMA-százalékos érzékenység (HOMA‐% S)) indexértékek.
Következtetés
C57BL/6J hím egerek 9 hetes HFD-n, 60 kcal energiát szolgáltatva a zsír megjelenítéséből, károsodott az inzulinérzékenység és a krónikus gyulladás, így ez a DIO egérmodell alkalmas az elhízással összefüggő patológia korai stádiumainak tanulmányozására.
1. BEMUTATKOZÁS
A zsírszövet aktív endokrin szerv, amely érzékeli a tápanyag állapotát és szabályozza az energia mobilizálódását. 1 Bár a genetikai hajlam szerepet játszik, az elhízás nagyrészt az energiafogyasztás és az energiafogyasztás közötti egyenlőtlen egyensúly következménye, mivel az étkezési zsírbevitelt tekintik az adipozitás növekedésének fő tényezőjének. 2 Az elhízást az adipocita halál, a zsírszöveti makrofágok (ATM) és a monociták beszűrődése, a zavart adipocita differenciálódás és szekréció, valamint a krónikus gyulladás jellemzi. Az elhízás több társbetegséggel jár együtt, mint például májbetegség, metabolikus szindróma és 2-es típusú diabetes mellitus.
Ennek a vizsgálatnak a célja a 60% zsírtartalmú étrend 9 héten át tartó hatásának vizsgálata hím C57BL/6J egerekben. QUICKI és HOMA2 indexek segítségével értékeltük a morfológiai jellemzőket (testtömeg és hasi kerület), a WAT és a barna zsírszövet (BAT) raktárait, a májzsír felhalmozódását, a keringő proinflammatorikus citokinek plazmaszintjét, valamint az inzulinrezisztenciát.
2. ANYAGOK ÉS MÓDSZEREK
2.1 Állatok
Az in vivo kísérletet a National Institutes of Health (NIH) irányelveinek megfelelően hajtották végre, a Feinstein Institute for Medical Research, Northwell Health, Manhasset, New York intézményi állatgondozási és felhasználási bizottságának (IACUC) jóváhagyott protokollja alapján.
Hat hetes C57BL/6J DIO Control (készlet: 380056) és C57BL/6J DIO (készlet: 380050, The Jackson Laboratory) hím egereket izokaloros, alacsony zsírtartalmú kontroll étrendre (zsírból 10% kcal energiára) helyeztünk (kutatási diéták, Cat. # D12450B) (rendszeres étrend (RD) csoport) vagy HFD (60% kcal zsírtartalmú energia) (Research Diets, Cat. # D12492) (HFD csoport), illetve 12 hetes korukban a A Feinstein Orvosi Kutatóintézetek, ahol az étrend 15 hetes életkorig folytatódott. Az alkalmazott étrendek teljes összetételét és kalóriatartalmát az S1 és S2 táblázat tartalmazza. Az egereket halálos dózisú CO2-nak kitettük, majd méhnyak elmozdultuk.
2.2 Vérvétel, valamint glükóz- és adipokinmérés
Az egereket egy éjszakán át (14-15 óra) éheztettük. Vérmintákat vettek az arcvénából reggel, közvetlenül az áldozat elõtt, és a OneTouch Verio Flex ™ System (LifeScan) alkalmazásával mértük a glükózszintet. Ennek a rendszernek a regressziós statisztikája a következő: 95% CI meredekség = 0,97-1,01; 95% CI elfogás = -1,59-7,55 mg/dl; standard hiba (Sy.x) = 14,0 mg/dl; R 2 = .98. Feláldozás után a terminális vérmintákat szívpunkcióval vettük 5,4 mg EDTA-t (BD) tartalmazó csövekbe. A mintákat 3 órán át azonnal jégre helyeztük, és 5000 ° C-on centrifugáltuk g/ 15 perc/4 ° C-on a plazmafrakció szétválasztásához, majd a mintákat alikvotáljuk és azonnal –86 ° C-on lefagyasztjuk további feldolgozásukig. Az IL-6, inzulin, leptin, MCP-1, PAI-1 (összesen), rezisztin és TNF-α plazmaszintjét Luminex assay-vel mértük MILLIPLEX Map Mouse Adipokine Magnetic Bead Panel ‐ Endokrin Multiplex Assay (Millipore, Cat. # MADKMAG ‐ 71K). A vizsgálat érzékenysége, pontossága és pontossága a következő volt: az érzékenység (minimális kimutatható koncentráció (MinDC) [pg/ml], MinDC + 2SD [pg/ml]): IL-6 (2,3, 6,3), inzulin (13,0, 27,7), leptin (4,2, 8,2), MCP-1 (4,9, 11,9), PAI-1 összesen (4,0, 10,3), rezisztin (1,1, 3,7), TNF-α (5,3, 11,0); pontosság (intra-assay% CV, inter-assay% CV) mind a hét elemzett
2.3 Az inzulinérzékenység értékelése egerekben
Az inzulinérzékenységet kvantitatív inzulinérzékenység-ellenőrző index (QUICKI) (1/log inzulin (mU/L) + log glükóz (mg/dL)) 6 és homeosztázis modell-értékelés (2) (HOMA2) index alkalmazásával értékeltük online alapú számológéppel az Oxfordi Egyetem Diabetes Trials Unit-je (https://www.dtu.ox.ac.uk/homacalculator/), amely értékeket ad az inzulinrezisztencia (HOMA ‐ IR), az egyensúlyi állapotú β ‑ sejt funkció (HOMA ‐%) B) és inzulinérzékenység (HOMA -% S).
2.4 A szövet boncolása és előkészítése
Az állatokat perfundáltuk formaldehiddel, és különféle zsírszövetraktárakat (epididymális, inguinalis, mesenterialis, interscapularis, retroperitoneális, pericardialis WAT és interscapularis BAT) és a májat boncoltunk, súlyoztunk és PBS-ben tároltunk. A mintákat paraffin beágyazás, szeletelés, valamint hematoxilin és eozin (H&E) festés céljából a New York-i New York-i Egyetem Orvostudományi Karának hisztopatológiai központjába küldték.
2.5 A máj lipidfelhalmozódásának értékelése
A máj lipid felhalmozódását a lipid tartalmú hepatociták számának megszámlálásával értékeltük. Az adatokat a lipidtartalmú hepatociták százalékos arányában adjuk meg mikroszkopikus látómezőnként.
2.6 Statisztikai elemzések
A statisztikai elemzéseket GraphPad Prism 7 szoftver (GraphPad Software) segítségével végeztük. Statisztikailag szignifikáns különbséget két csoport (RD és HFD) átlaga között a Student's segítségével számoltunk ki t teszt és kétfarkú eloszlás. Az eredményeket statisztikailag szignifikánsnak tekintettük, ha P ≤ .05. Az eredményeket átlag ± SEM-ként adtuk meg.
3 EREDMÉNYEK
3.1 Testtömeg és zsírszövet
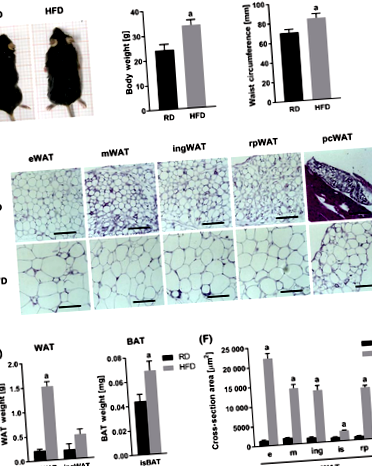
HFD-vel táplált egerek voltak kiállítva
A testtömeg 40% -os növekedése (1. táblázat, valamint 1A. És B. Ábra) és
A hasi kerületük 20% -kal növekszik (1. táblázat és 1C. Ábra). Különböző WAT (epididymális WAT (eWAT), mesenterialis WAT (mWAT), inguinalis WAT (ingWAT), retroperitoneális WAT (rpWAT) és pericardialis WAT (pcWAT)) és BAT (interscapularis (isBAT)) depót boncoltak és elemeztek (1D ábra) ). A HFD csoport egerekben a testtömeg növekedése elsősorban az eWAT felhalmozódásának volt köszönhető (1. táblázat és 1E. Ábra). Jelentős növekedést észleltek a zsírfelhalmozódásban az isBAT depóban is (1. táblázat és 1E. Ábra). Az összes vizsgált WAT depóban a HFD-kezelés az adipocita méretének jelentős növekedését eredményezte (1D., F és 1. ábra).
3.2 Máj
A HFD-vel táplált egereknél nagyobb máj alakult ki (2A. Ábra), amelyek lényegesen nehezebbek voltak, mint az RD csoportos egereké (1. táblázat és 2B. Ábra). Vizuálisan a HFD-vel táplált állatok májait megkülönböztettük az RD csoportba tartozó egerek halvány színétől (2A. Ábra). A szövetlemezek mikroszkópos vizsgálata nagyobb mértékű hepatocita lipidcsepp felhalmozódást mutatott ki a HFD májából, mint az RD csoportból származó májban (2C. És D ábra és 1. táblázat).
3.3 Krónikus gyulladás
Az elhízás jellemzője az adipocita halálozás gyakoribb előfordulása, valamint a koronaszerű struktúrákat (CLS) alkotó monociták és makrofágok beszivárgása (3A. Ábra). A WAT-minták vizsgálata a HFD-vel táplált egerek WAT-ban magasabb CLS-jelenlétét mutatta, mint az RD-n (3B. Ábra és 1. táblázat). A HFD csoportba tartozó egereknél a proinflammatorikus citokinek (tumor nekrózis faktor-alfa (TNF-α), interleukin-6 (IL-6), leptin, monocita kemoattraktáns protein-1 (MCP-1), plazminogén - bazális keringési szintje is szignifikánsan magasabb volt. aktivátor inhibitor ‐ 1 (PAI ‐ 1) és rezisztin) (3C. ábra és 2. táblázat).
| TNF-α [pg/ml] | 6,60 ± 0,73 | 12,62 ± 0,50 | .0209 |
| IL-6 [pg/ml] | 15,95 ± 4,97 | 59,95 ± 6,43 | .0002 |
| Leptin [ng/ml] | 0,45 ± 0,10 | 11,27 ± 2,68 | .0024 |
| MCP-1 [pg/ml] | 12,57 ± 4,22 | 27,69 ± 4,45 | .0328 |
| PAI ‐ 1 [ng/ml] | 1,46 ± 0,12 | 2,36 ± 0,31 | .0151 |
| Rezisztin [ng/ml] | 0,77 ± 0,04 | 2,04 ± 0,29 | .0008 |
- Értékei P A ≤ .05 félkövérrel van jelölve.
- Rövidítések: RD, rendszeres étrend; HFD, magas zsírtartalmú étrend; TNF-α, tumor nekrózis faktor-alfa; IL-6, interleukin-6; MCP ‐ 1, monocita kemoattraktáns protein ‐ 1; PAI ‐ 1, plazminogén aktivátor inhibitor ‐ 1.
3.4 Inzulinérzékenység
Az éhomi vércukorszint és a plazma inzulinszint egyaránt szignifikánsan megemelkedett a HFD csoportba tartozó egerekben (4A. Ábra és 3. táblázat). Ezen mérések alapján kiszámítottuk az inzulinrezisztencia-indexet kvantitatív inzulinérzékenység-ellenőrző index (QUICKI) és homeosztázis-modell értékelés (HOMA) index felhasználásával. A HFD-vel táplált egerek alacsonyabb QUICKI és magasabb HOMA-inzulinrezisztencia (HOMA-IR) indexeket mutattak (4B. És C. Ábra és 2. táblázat). Bár a HOMA index (HOMA-% β-sejtek (HOMA-% B)) alapján számított tendencia mutatkozott a károsodott β-sejtek működésében, nem találtunk statisztikailag szignifikáns különbséget a két állatcsoport között ( Ábra és a 3. táblázat). A HFD csoportba tartozó egerek jelentősen csökkent inzulinérzékenységet mutattak a HOMA index (HOMA% érzékenység (HOMA% S)) értékei alapján (4C. Ábra és 3. táblázat).
4. MEGBESZÉLÉS
A DIO egérmodellek felbecsülhetetlen értékűnek bizonyultak a krónikus gyulladásos és inzulinrezisztencia vizsgálatokban. Különböző HFD egér-modellek vannak elhízással, inzulinrezisztenciával, különböző patofiziológiai válaszokkal. Itt megvizsgáltuk a 9 hetes HFD-etetés hatását hím C57BL/6J egereknél 60% zsíros energiát biztosító étrenddel az inzulinrezisztencia és a krónikus gyulladás kialakulására. Megállapítottuk, hogy ez az állatmodell alkalmas lehet olyan vizsgálatokra, amelyek célja az elhízással összefüggő patológia viszonylag korai szakaszát megcélzó megelőzési és kezelési megközelítések vizsgálata.
KÖSZÖNETNYILVÁNÍTÁS
Ezt a munkát Gerald J. és Dorothy R. Friedman New York-i Orvosi Kutatási Alapítvány támogatásai támogatták.
- Küzdelem a PCOS-szal diétával Átfogó inzulinrezisztencia-diétakönyv azoknak a nőknek, akiknek PCOS-val küzdenek
- A ketogén étrend hosszú távon csökkenti-e az inzulinrezisztenciát?
- A magas zsírtartalmú étrend által kiváltott szívműködési zavarok a megváltozott szívizom inzulinhoz kapcsolódnak
- Fogyókúra és gyulladás a bőrgyógyászatban - Gyakorlati bőrgyógyászat
- Alacsony kalóriatartalmú, magas fehérjetartalmú és alacsony kalóriatartalmú normál fehérjetartalmú étrend összehasonlítása a derék kerületén