Diétás hiperoxaluriától származó Cureus krónikus nefropátia A vesefunkció tartós javulása után
Közzétett: 2017. március 20. (Az előzmények megtekintése)
DOI: 10.7759/healus.1105
Idézd ezt a cikket: Sun Y, Horowitz B L, Servilla K S és mtsai. (2017. március 20.) Krónikus nefropátia az étrendi hiperoxaluriából: a vesefunkció tartós javulása az étrendi beavatkozás után. Cureus 9 (3): e1105. doi: 10,7759/healus.1105
Absztrakt
Bevezetés
A hiperoxaluria urolithiázt, nephrocalcinosist, akut vesekárosodást (AKI) és krónikus vesebetegséget (CKD) okozhat. A vizelettel kiválasztott oxalát mind az endogén termelésből, mind a gasztrointesztinális felszívódásból származik. Az oxalátok fokozott endogén termelésével lehet találkozni primer hiperoxaluria esetén, vagy nagy mennyiségű oxaláttá metabolizált vegyületek, például aszkorbinsav és etilén-glikol elfogyasztása után. Az oxalátok fokozott emésztőrendszeri felszívódása bizonyos bélbetegségeknél és/vagy műtéti beavatkozásoknál tapasztalható, amelyek steatorrhea-t (bél hyperoxaluria) okoznak, vagy magas oxalát tartalmú ételek (diétás hiperoxaluria) bevitele után. Az urolithiasisban társuló enyhe hiperoxaluria egyik típusát idiopátiásnak nevezik, mivel annak patogenezisét nem határozták meg végérvényesen.
A vizelettel történő oxalátkiválasztás mértéke nyomokat adhat a hiperoxaluria etiológiájáról. Az oxalát kiválasztás jellemzően nagyon magas primer hiperoxaluria esetén, az étrendi oxalát bevitelétől függ enterális hiperoxaluriában, és állítólag valamivel magasabb, mint a normál tartomány (90 mg/24-óra; B) enterális hiperoxaluria> 90 mg/24-óra; C) idiopátiás hiperoxaluria 1. ábra: Gallium szcintigráfia
A kép összhangban áll az intersticiális nephritisrel. A vesék még az alkalmazás után 72 órával is visszatartották az izotópot.
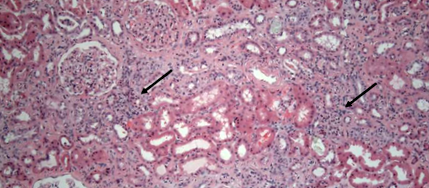
A rabeprazol-kezelést abbahagyták, és az orális prednizont elkezdték. A vizeletvizsgálat azonban továbbra is pyuria-t, fehérvérsejt-gátlást és szerény proteinuria-t mutatott, miközben a szérum kreatinin-koncentrációja továbbra is 4,19 mg/dl magasra emelkedett (a becsült eGFR a vesebetegség étrendjének módosításával számítva (MDRD) - 15 ml/perc/1,73 m2 testfelület (BSA)). Ekkor perkután vese biopsziát végeztek. A szövettanon nem volt glomeruláris patológia. A tubulusok a hám fokális ellapulását és a hámsejtek vakuolizációját mutatták. A biopsziás minta körülbelül 60% -a tubuláris atrófiát és intersticiális fibrózist mutatott trichrom folton. Mérsékelt artériás és arterioláris sclerosisról is beszámoltak. Az interstitiumban mononukleáris sejtek fókuszsűrű infiltrátumait láthattuk (nyilak a 2. ábrán).
2. ábra: Vese biopszia
Számos kalcium-oxalát-kristály, amelyek polarizált fény alatt kettős törést mutatnak, és néhány tubulus lumenében néhány kalcium-foszfát-kristály látható (3. ábra).
3. ábra: Vese szövettana
A képen oxalát-lerakódások láthatók.
Az immunfluoreszcencia kimutatta az IgM és a C3 szegmentális lerakódását a mezangiumban, szétszórt fibrin lerakódásokat az interstitiumban, és a C3 fokális lerakódását a tubuláris alapmembránokban. Az elektronmikroszkópia megerősítette a hám jelentős degeneratív elváltozásait. A glomerulusok csak az interdigitáló lábfej fokális elválasztását mutatták. Elektronsűrű lerakódásokat nem találtunk. A kóros diagnózis egy hiperoxalurikus állapot volt, krónikus interstitialis nephritis, elterjedt kalcium-oxalát lerakódás a tubulusokban, markáns tubuláris duzzanat és tubuláris sérülés jelei.
1. táblázat: A vizelet kiválasztási aránya magas és alacsony oxalát bevitelnél
A szérum kreatinin-koncentráció 3,02 ± 0,13 mg/dl volt a magas oxalátfogyasztás időszakában, és 2,34 ± 0,39 mg/dL az alacsony oxalátfogyasztás korai szakaszában, amikor a 24 órás vizeletgyűjtés történt. 1. felső index: Két vizeletgyűjtemény. 2. felső index: Négy vizeletgyűjtemény. 3. felső index: Egy vizeletgyűjtés.
| Változó | Normál tartomány | Magas oxalát beviteli periódus | Alacsony oxalát beviteli periódus |
| Térfogat, L/24 óra | 1,0 - 2,0 | 3,7 ± 1,0 1 | 5,1 ± 1,0 2 |
| Kreatinin, mg/24 óra | 800 - 2 000 | 1 455 ± 485 1 | 1 576 ± 340 2 |
| Oxalát, mg/24 óra | 1 | 36 ± 4 2 | |
| Oxalát/kreatinin, mg/g | 1,6 - 37 | 228 ± 98 1 | 36 ± 5 2 |
| Citrát, mg/24 óra | > 320 | 84 ± 25 1 | 105 ± 15 1 |
| Kalcium, mg/24 óra | 3 | 85 ± 35 1 | |
| Foszfor, mg/24 óra | 3 | 1,120 3 | |
| Húgysav, mg/24 óra | 1 | 389 ± 52 1 |
Vita
Ez az eset két fő szempontot vet fel. Az első pont az, hogy a magas oxaláttartalmú élelmiszerek krónikus bevitele hiperoxaluriához vezethet, a vizelet oxalátjának kiválasztásával hasonló mértékben, mint az elsődleges hiperoxaluriában. A vizelet oxalátkiválasztásának a gyomor-bél felszívódásából származó összetevőjét az étrend oxaláttartalma és az oxalát felszívódási sebessége határozza meg a belekben. A magas oxaláttartalmú élelmiszerek közé tartoznak a leveles zöldségek, például a spenót, a különböző diófélék, például a földimogyoró, és a trópusi gyümölcsök, beleértve az Averrhoa carambola (csillaggyümölcs) és az Averrhoa bilimbi.
Az átlagos napi étrendi oxalátfogyasztás az Egyesült Államokban 214 mg a férfiaknál, 185 mg az idősebb nőknél és 183 mg a fiatalabb nőknél; a spenót az oxalátbevitel> 40% -át teszi ki [2]. A bélből történő oxalát felszívódásának magas szintjéhez vezető tényezők közé tartoznak az orvosi állapotok vagy a steatorrhoához vezető műtéti beavatkozások, az alacsony kalcium- és magnézium-étrend-tartalom, amelyek mind megkötik az oxalátot a gyomor-bél traktusban, mind pedig csökkentik annak felszívódását és a vesén keresztüli kiválasztódását, valamint bizonyos baktériumfajok, különösen az Oxalobacter formigenes, anaerob baktérium hiánya a bélflórából, amely metabolizálja az oxalátot. Ennek a baktériumnak a bélből való hiánya hyperoxaluriával társult. Az Oxalobacter formigenes készítmények beadása hasznos lehet hiperoxalurikus állapotokban, ideértve az elsődleges hiperoxaluriát és az enterális hiperoxaluriát.
Noha az egyének között jelentős eltérések vannak, a vizelet oxalát kiválasztása az étrendi oxalát bevitelével párhuzamosan növekszik, ha más, az oxaluriát potenciálisan befolyásoló változók kontroll alatt állnak [3]. Az oxalátbevitel mellett az oxalát-prekurzorok bevitele hyperoxaluriát okozhat. Az aszkorbinsav, a piridoxilát, amely a glioxilsav és a piridoxin kombinációja, és a hidroxiprolin az oxalát lehetséges forrásai, amelyek klinikai és kísérleti vizsgálatokban hiperoxalurikus vesebetegséget okoztak. Végül hyperoxaluria és oxalát nephropathia alakulhat ki a parenterális gyógyszerek oxalátsóinak eredményeként.
Élelmiszerek, gyógyszerek vagy magas oxaláttartalmú mérgező anyagok elfogyasztása esetén bekövetkező akut mérgezés fő megnyilvánulása magában foglalja a gyomor-bél traktust (fájdalom, hányinger, véres hányás, véres hasmenés), az idegrendszert (tetania, az agyödéma megnyilvánulása) és a vesék (proteinuria, oligo-anuria). A túlélő AKI-betegek helyreállíthatják a normális vesefunkciót akkor is, ha súlyos veseelégtelenségük alakul ki, amely egy ideig dialízist igényel [4-6].
A CKD az étrendi hiperoxaluria következményeként alakulhat ki. A hiperoxalurikus CKD oka egy földimogyoró fogyasztása volt egy betegnél [7] és három másik betegnél a „gyümölcslevek” (nagy mennyiségű, különböző zöldségekből kivont gyümölcslé krónikus bevitele) [8]. Az oxalátkristályok lerakódása a vese tubulusokban, a tubulusok kiterjedt degeneratív változásai, valamint az interstitialis gyulladás és a fibrózis változó mértéke volt a nephropathia fő szövettani jellemzője ezekben az esetekben. A vesefunkció javult a magas oxalátbevitel abbahagyása után [7-8].
Az étrendi hiperoxaluriából származó CKD hasonló szövettani jellemzőkkel rendelkezik, mint az oxalát nephropathia minden más típusa. Steril pyuria fehérsejtes gipszekkel az interstitialis nephritis minden típusában megtalálható. Érdekes, hogy a kalcium-oxalát kristályokat, amelyek a klinikusokat az oxalát-nephropathia diagnosztizálása felé terelhetik, nem láttuk betegünk vizeletében, vagy több publikált oxalát-nephropathiás jelentésben.
A gallium szcintigráfiát alkalmazták az akut interstitialis nephritis és az AKI egyéb típusainak megkülönböztetésére. Nem találtunk jelentést gallium szcintigráfiáról hiperoxalurikus betegeknél. Betegünknél a gallium szcintigráfia pozitív volt, ami alátámasztotta az interstitialis nephritis kezdeti klinikai diagnózisát. A klinikai kép, a vizeletvizsgálat és a képalkotó módszerek általában nem elegendőek az oxalát nephropathia és az interstitialis nephritis egyéb típusainak megkülönböztetéséhez. Vese biopszia szükséges. A C3 és az immunglobulinok lerakódását a tubuláris alapmembránban enterális hiperoxaluriában is találták [4].
A tubuláris hámkárosodás és az interstitialis gyulladás molekuláris mechanizmusainak új fejleményei rávilágítottak az oxalát nephropathia mechanizmusára. A veseszövetekben oxalátkötő fehérjéket és a kalcium-oxalát tubuláris sejtekhez való kapcsolódásának mediátorait jellemezték. A hiperoxaluria a vese-sérülés molekula-1 (KIM-1) up-szabályozását okozza. Megállapították, hogy a vizelet oxalát szintje korrelál a tumor nekrózis faktorral és a Fas ligandum szinttel, és összefüggést mutat a vese tubuláris sejtek apoptózisával. A gyulladásos sejtek nagy molekulatömegű citoszolos komplexek, amelyek a veleszületett immunrendszer részét képezik. A nukleotidkötő domén, a leucinban gazdag gyulladás (NALP3 vagy NLRP3 vagy kriopirin) aktiválódás után oligomerizálódik, és proteáz-kaszpáz 1-et toboroz, hogy gyulladásos fehérje-komplexet képezzen. Az aktivált 1 kaszpáz hasítja az IL-1β és az Il-18 inaktív prekurzorait, ami ezen citokinek aktív formáinak kialakulásához vezet. Kísérleti állatokon végzett vizsgálatok azt mutatták, hogy a hiperoxaluria aktiválja a NALP3 gyulladását, és hogy a NALP3 által közvetített gyulladás szükséges az oxalát nephropathia CKD kialakulásához [9].
Az esettanulmány által illusztrált második fontos pont az, hogy az étrendi hiperoxaluria felismerése és az oxalátbevitel csökkentése a vesefunkció javulásához vezethet, ami évekig fennmaradhat. A diétás hiperoxaluria ideális szubsztrátumot kínál az oxaluria normalizálásának a hiperoxalurikus CKD lefolyására gyakorolt hatásának tanulmányozásához, mert esetünkben a hiperoxaluria egyetlen oka a magas étrendi oxalátfogyasztás volt. Két korábbi jelentés [7-8] észlelte a vesefunkció javulását az oxalátbevitel normalizálása után. Jelentésünk azt jelzi, hogy még akkor is, ha a CKD előrehaladott stádiumba került, a diétás hiperoxaluriában a vesefunkció javulása az oxalátbevitel csökkentése után fenntartható és jelentős lehet, ami a szérum kreatinin és a vizelet eredményeinek normalizálásához vezet. A CKD részleges javulásáról beszámoltak olyan betegeknél is, akiknél előrehaladott hiperoxalurikus CKD volt, mivel nagy mennyiségű aszkorbinsav krónikus bevitele következett be.
Következtetések
Vese biopsziára van szükség az étrendi hiperoxaluria miatt másodlagos CKD diagnózisának megállapításához. Az étrendi hiperoxaluria miatt másodlagos CKD-s betegeknél az alacsony oxaláttartalmú étrend bevezetése az oxalát vizeletürítésének csökkenéséhez vezet, és a vese üledékének gyors normalizálódásához és a vesefunkció lassú javulásához vezethet. Az étrendi hiperoxaluria megelőzésének, a magas oxaláttartalmú ételek vagy azok prekurzorainak túlzott fogyasztásának elkerülésével, a lakosság étrend-oktatásának részét kell képeznie.
- Diétás megközelítések a magas vérnyomás megállításához és a krónikus vesebetegség kockázata Szisztematikus áttekintés és
- A vese ischaemia előtti étkezési fehérje jelentősen befolyásolja a postischaemiás urémiát
- A metabolikus acidózis diétás kezelése krónikus vesebetegségben
- Az étrendi fehérjebevitel hatása a szérum teljes CO2 koncentrációjára krónikus vesebetegségben
- Krónikus veseelégtelenség macskáknál - Új Plymouth Vet Group