Boldenone
Kapcsolódó kifejezések:
- Anabolikus szteroid
- Metiltesztoszteron
- Nandrolone
- Androgén
- Stanozolol
- Oximetolon
- Tesztoszteron
- Androsztanolon
- Férfi típusú alopecia
Letöltés PDF formátumban
Erről az oldalról
Az állat-egészségügyi toxikológia szabályozási szempontjai
A közegészségügyre nézve tiltott állatorvosi gyógyszerek
Az embereknél tiltottan alkalmazott, jóváhagyott állat-egészségügyi gyógyszerek közé tartozik a boldenon (egyensúly), a ketamin, a sztanozolol (Winstrol) és a trenbolon (Finajet). Az anabolikus szteroidokat tartalmazó állatgyógyászati termékek, amelyeket kizárólag szarvasmarháknak vagy más, nem emberi fajoknak implantátumokkal történő beadására szántak, és amelyeket a CVM, az USA FDA jóváhagyott, nem tartoznak az összes menetrend hatálya alá (Drug Enforcement Agency: 21 CFR Parts 1300–1316, List ütemezési tevékenységek és szabályozott anyagok (1999b; kábítószer-fogyasztás, 1997).
A „különleges k” és „k” néven ismert ketamin-hidroklorid általános érzéstelenítő emberi és állatorvosi alkalmazásra. A ketamin a pentaklór-fenolhoz (PCP) hasonló hatásokat produkál a lizergsav-dietilamid (LSD) vizuális hatásaival együtt. Az utcán értékesített ketamin eltérített törvényes ellátásból származik, elsősorban állatorvosi klinikákból. Megjelenése hasonló a gyógyszerészeti minőségű kokainéhoz, és horkolnak, alkoholtartalmú italokba teszik vagy marihuánával kombinálva füstölik. A ketamin-visszaélések gyakorisága növekszik. A ketamint 1999 augusztusában az ellenőrzött anyagokról szóló törvény (CSA) III. Jegyzékébe helyezték (Drug Enforcement Agency: 21 CFR Parts 1300–1316, Schedules of Controlled Substances, 1999a).
Hiperandrogenizmus, hiperinsulinémiás
Az androgéntermelés helyszínei
Az androgének C19 szteroidok, amelyek enzimes hasítás révén koleszterinből származnak. A bőr területén szabadon keringő tesztoszteron és dehidrotesztoszteron az aktív molekula, míg a DHEA gyenge androgénnek számít. A tesztoszteron termelésének fő helyei a petefészek theca és a stroma sejtek. A DHEA-t a mellékvese termeli. Jelentős androgéntermelés és anyagcsere fordul elő a szubkután zsírban. Az androgéntermelés pubertáskor kezdődik, és másodlagos nemi jellemzőkkel, a szemérem- és hónaljszőrzet kialakulásával függ össze. A premenopauzás nőknél a petefészek az androgének fő forrása. Az ösztrogén és az androgén közötti egyensúly fenntartja a haj eloszlását és a haj típusát (vékony vagy durva).
Endokrinológia
Androgének
A nőstényben az androgének szintetizálódnak mind a petefészek, mind a mellékvesékben. A keringő tesztoszteron 25% -a közvetlenül a petefészekben képződik. A maradék vagy közvetlenül a mellékveséből származik (25%), vagy közvetetten elsősorban az androszténdion (50% a petefészek és 50% a mellékvese) és sokkal kisebb mértékben a dihidroepiandrostenedion (DHEA, elsősorban a mellékvesék). A nőstényben az androgének valószínűleg felelősek a szemérem- és hónaljszőrzet fenntartásáért, és kontrollálják a libidót is.
A haj és a köröm betegségei
Mintás alopecia (androgén alopecia)
Az androgén alopecia progresszív betegség, amely idővel súlyosbodni kezd. Az androgenetikus alopecia orvosi kezelése magában foglalja a nőknél a 2% -os topikális minoxidilt és a férfiaknál az 5% topikális minoxidil 2-t vagy az orális finaszteridet, napi 1 mg-ot. 3 A klinikai javulás leginkább a már meglévő haj megvastagodásának köszönhető.
Az androgenetikus alopecia kezelését legalább hat hónapig folytatni kell, mielőtt felmérnék hatékonyságukat, és az eredmények fenntartása érdekében a rendszeres gyógyszerhasználat kötelező. A minoxidil megszakításával akut telogén effluvium keletkezik, amely 3-4 hónapos megszakításként nyilvánvalóvá válik, és egyidejű finaszterid-kezeléssel nem lehet megakadályozni. A finaszterid megszakítását fokozatos hajhullás követi, és 1 év után visszatér az előkezelés állapotába. A hajátültetés jó lehetőség súlyos androgenetikus alopeciában szenvedő férfiak számára, és a napi 1 mg finaszterid-kezelés javítja a műtét hosszú távú eredményeit. A nők hajátültetése bonyolultabb, mert a hajritkulás a parietalis és az occipitalis régióban gyakran diffúz, ezért nincs jó hajdonor terület. Ezenkívül a műtét előidézheti a már meglévő haj kiürülését a befogadó területén, ami nőknél a haj elvékonyodásának jelentős átmeneti romlását eredményezi.
Nemi hormonok és az immunrendszer
Verthelyi Daniela, a Hormonok enciklopédiájában, 2003
V Androgének
Az androgénreceptor expresszióját dokumentálták a thymus és a csontvelő limfoid és nonmfoid sejtjeiben, de kifejlett érett perifériás limfocitákban továbbra is ellentmondásos. Ez az expressziós mintázat arra utal, hogy az androgének fő hatásának inkább a T és B limfociták fejlődési érésén kell lennie, mint az érett effektor sejteken. Az ösztrogénekhez hasonlóan az androgének is a CD4 + CD8 + (DP) timociták apoptózisával indukálják a csecsemőmirigy involúzióját, amelyet a megnövekedett helyi TNFα és a csökkent IL-3 közvetít. A hím egerek prepubertális kasztrálása a thymus hipertrófiáját indukálja. Az így létrejövő csecsemőmirigy megtartja normális felépítését, de megnövekedett a sejtjei (főleg a DP éretlen timocitáinak szaporodása miatt). Az androgének beadása blokkolja az éretlen T-sejtek szaporodását. A hím egerek kasztrálása a pre-B-sejtek populációjának terjeszkedését is eredményezi a csontvelőben, amelyet a tesztoszteron vagy dehidrotesztoszteron kezelés megfordíthat. Annak ellenére, hogy a perifériás érett immunsejtekben nyilvánvalóan hiányzik az androgén receptor, a kasztrált hím egereknél a lép tömegének 40% -os növekedése figyelhető meg.
In vitro az androgének fokozzák a CD8 + T-sejtek aktivitását, amit a lépsejtek csökkent proliferációja bizonyít a PHA hatására. Ezen túlmenően a nők fitohemagglutininnel stimulált limfocita tenyésztési felülúszóinak magasabb szintje az IFN-γ és IL-2, valamint alacsonyabb IL-4 és IL-10 szint kiválasztódik a nőkhöz képest. Egerekben az in vivo kezelés vagy a limfociták androgéneknek való közvetlen kitettsége az IL-2 fokozott termeléséhez vezet. Az androgének nagy dózisban is csökkentik (vagy alacsony dózisban növekednek) a TNFα szekrécióját és a makrofágok nitrogén-oxid szintézisét. A B-sejteken az androgének csökkentik az Ig szekréciót és a pokeweed mitogénre adott proliferatív reakciókat. Ez a hatás részben függ az IL-10 szekréciójától, de független a sejtdonor hormonális állapotától (hím vagy nő; a menstruációs ciklus luteális vagy follikuláris fázisa; posztmenopauzális).
Az ösztrogénekkel ellentétben az androgének számos autoimmun betegség lefolyására kedvezően hatnak. Ezt kísérleti autoimmun encephalitis, adjuváns ízületi gyulladás és szisztémás lupus erythematosus (SLE) állatmodelljeiben mutatták be. A védőhatásokat az 1-es típusú immunválasz felé történő elmozdulás, a csökkent B-sejtaktivitás alacsonyabb Ig-szekrécióval és a gyulladásgátló citokinek csökkentett szekréciója közvetíti a makrofágok által. Ezek a biztató eredmények számos folyamatban lévő klinikai vizsgálathoz vezettek sclerosis multiplexben és SLE-ben szenvedő betegeknél.
Dopping, a hajelemzés alkalmazásai
10.2.3 S1.1.b: Endogén AAS-ok
Ez az anyagcsoport tartalmazza a dedikált vegyületek pozitív listáját, amelyeket tiltottnak tekintenek. Számos úgynevezett prohormon (androsztenedion, androsztenediol) volt legálisan elérhető 1990-ben, és táplálékkiegészítőként nagyon népszerűvé vált. Ezek a gyógyszerek gyenge biohasznosulásban szenvedtek, és széles körben lényegtelenné váltak, miután bekerültek az ütemezett III gyógyszerek listájába (US Controlled Substance Act [21]). Az endogén anabolikus szteroid, amely a legjelentősebb visszaélési potenciállal rendelkezik, a tesztoszteron, amely injekciós észterek formájában kapható (acetát, propionát, cypionát, izokaproát, izobutirát, fenilpropionát, enantát, fenilpropionát, dekanoát, undekanoát) injekciós tesztoszteron szuszpenzióként, tesztoszteron gél tapaszok és tesztoszteron-undekanoát orális kapszulák. Ezenkívül a dehidrotesztoszteronnak és a dehidroepiandioszteronnak (DHEA) csak kis jelentősége van, amelyek egyes országokban, köztük az Egyesült Államokban, továbbra is legálisan elérhetők.
Mint minden esetben, amely az endogén vegyületekkel foglalkozik, kihívást jelent a bazális szintek megkülönböztetése a bántalmazástól. Feltételezzük, hogy az endogén szteroidok küszöbértékek alapján történő értékelése kevésbé érzékeny és potenciális bírósági vita tárgya, mint az exogén vegyületek közvetlen azonosítása.
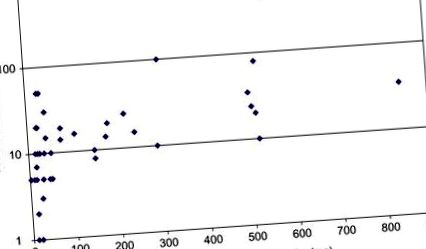
10.4. Ábra A tesztoszteron-észterek és a szabad tesztoszteron hajkoncentrációinak összefüggése. A depó készítmények intramuszkuláris injekciója a szabad tesztoszteron mérsékelt növekedését eredményezi a hajban. Az 500 pg/mg szabad tesztoszteront kimutató tényező a szabad tesztoszteron (nagyon atipikus) injekciójának volt köszönhető.
A szérumban, a hajban, a szájüregben, az izzadságban és a mecóniumban alkalmazott visszaélések gyógyszereinek elemzése
Egyéb gyógyszerek elemzése
Sok más gyógyszert, köztük opiátokat, fenciklidint (PCP), benzodiazepineket, barbiturátokat, gamma-hidroxi-butirátot, ketamint, anabolikus szteroidokat és zolpidemet elemeztek hajmintákban, GC/MS vagy LC – MS/MS alkalmazásával. Baumgartner és mtsai. szintén elemezte a haj PCP-jét hét alanynál, aki elismerte a PCP használatát. Valamennyi alany kimutatta PCP jelenlétét a hajban (0,3–2,8 ng/mg mosott haj), de csak egy személy mutatott pozitív PCP-t a vizelet toxikológiai elemzésében [15]. Egy másik, pszichiátriai betegeket használó vizsgálatban a hajelemzés 47 betegből 11-ben mutatott ki PCP-t. A vér- és vizeletvizsgálat negatív volt mind a 47 betegnél [16] .
Noha a GC/MS-t széles körben alkalmazzák a haj különböző kábítószereinek elemzésére, az LC – MS/MS egyre népszerűbb, mint választott módszer, mert sok különböző gyógyszerosztály elemezhető egy futtatásban derivatizálás nélkül is. Shah és mtsai. elemzett nandrolon, sztanozolol, tesztoszteron, boldenon, kokain, benzoilekgonin, kakaetilén, amfetamin, metamfetamin, MDMA, MDA, dezmetil-szelegilin, efedrin, THC, 11-hidroxi-THC, THC-COOH, ketamin, nor-ketamin, klenoluterol, terbutalin, szalbutamol, morfin, kodein és fenciklidin a hajmintákban diklór-metánnal végzett mosás, 1 M nátrium-hidroxid-oldattal történő emésztés, majd a gyógyszerek kivonása a belső standardokkal együtt az LC – MS/MS alkalmazásával végzett elemzéshez. A szerzők sztanozolol-d3, kokain-d3, MDMA-d5, THC-d3, kodein-d3, ketamin-d4 és PCP-d5 anyagokat használtak. A szerzők 233 emberi haj mintát elemeztek ezzel a módszerrel, és 70 önkéntes pozitívnak bizonyult egyes gyógyszereknél, de főleg visszaélések és szteroidok esetében. Bár 56 önkéntes 1 gyógyszer jelenlétét mutatta, más önkéntesek több gyógyszer jelenlétét mutatták (1 önkéntes pozitív volt 5 gyógyszer esetében) [17] .
Koster és mtsai. szintén használt LC – MS/MS amfetamin, metamfetamin, MDMA, MDA, MDEA, metilfenidát, kokain, benzoilecgonin, morfin, kodein, heroin, 6-monoacetil-morfin, metadon, 2-etilidén-1,5-dimetil-3, 3-difenil-pirrolidin (EDDP, metadon-metabolit), THC, nikotin és kotinin az emberi hajban. A szerzők módszerüket olyan betegek hajmintáinak elemzésére alkalmazták, akiket kábítószerrel való visszaélés miatt figyeltek. 47 beteg hajmintájában az analitikai határértéket meghaladó koncentrációban MDMA, metilfenidát, kokain, benzoilekgonin, kodein, metadon, EDDP, THC, nikotin és kotinin volt jelen. Az egyik beteg nagy mennyiségű kokain (38 762 pg/mg haj), benzoilekgonin (6052 pg/mg haj), metadon (14 402 pg/mg haj) és EDDP (1573 pg/mg haj) jelenlétét mutatta ki. 18] .
Nemi különbségek az autoimmun betegségekben
Specifikus autoimmun betegségek és nemek közötti különbségek
Szisztémás lupus erythematosus (SLE)
Az SLE-ben megváltozott szérum-hidroxilezett ösztrogénekről számoltak be. 3 Sőt, az SLE-ben a 17β-ösztradiolról kimutatták, hogy fokozza a sejtnövekedés és a proliferáció markereinek expresszióját, míg a tesztoszteron markerek indukálják a fokozott apoptózist. Kimutatták, hogy az ösztrogén fokozó szerepe az NF-κB út aktiválásával érvényesül. 40 Ezeket a megfigyeléseket RA-ban és az SLE-ben szenvedő betegek szinoviális szövetében mutatták ki. 40,41 Az RA és az SLE eredményei igazolják az androgének (tesztoszteron, dehidroxi-epiandroszteron vagy dehidrotesztoszteron) RA és antiösztrogének (ösztrogén receptor blokkolók vagy szelektív ösztrogén receptor modulátorok) SLE-ben történő alkalmazását. 42 Még várat magára, hogy az ösztrogén receptor antagonizmus meddőséghez vagy más nemkívánatos mellékhatásokhoz vezet-e a nőknél.
Orális fogamzásgátlók és SLE
Az enyhe aktív vagy inaktív betegségben szenvedő lupusos betegek többségének nincsenek fellángolásai kombinált (ösztrogén és progeszteron) orális fogamzásgátló szedése után. 43–45 Néhány ellenőrizetlen esetjelentés vagy bizonyos nyílt kísérletek szerint a lupusban fellángoló fellángolások jelennek meg nagy dózisú ösztrogének beadása után. 46,47 Az orális fogamzásgátlás biztonságosságát azonban közepesen aktív vagy súlyos lupus esetében nem vizsgálták kontrollált kettős-vak protokollban.
Ösztrogénreceptor-blokkolók az SLE-ben
Mivel az SLE-ben az ösztrogén szérum- vagy plazmaszintje nem különbözik az életkor és a nem szerinti normális kontrollaktól, 2 tanulmányt indítottunk az SLE perifériás vér mononukleáris sejtjeiben és az SLE-betegekből származó B-sejtvonalak ösztrogénreceptorainak (ER) jellemzésére és számszerűsítésére. 48 Eredeti munkánk nem mutatott mennyiségi különbségeket az SLE és a normálok között. 48,49 Sőt, az ösztrogén receptor kötődési affinitása az ösztrogénhez azonos volt az SLE-ben és a kontrollokban. 50
Az emberi SLE nemi különbségeihez vezető molekuláris mechanizmusokat megvizsgáltuk és nemrégiben felülvizsgáltuk. Egy nemrégiben készült jelentés szerint a nők SLE-túlsúlya a CD40 ligandum CD4 + T-sejteken történő demetilezésének tulajdonítható. A lupusban szenvedő nők inaktív X kromoszómájának demetilációja a CD40 ligandum túlexpresszióját eredményezte a CD4 + T sejteken. 25 Ez a T-B sejtek fokozott együttműködéséhez vezetne, az autoantitestek későbbi túltermelésével. Laboratóriumunkban a lupus T-sejtek ösztrogénnel történő aktiválását követően a CD40L túlzott expresszióját figyelték meg. Az ilyen túlzott expressziót az ösztrogén receptor blokkoló (fulvestrant) blokkolta. 9.
Rheumatoid Arthritis (RA)
A nőknél a reumás ízületi gyulladás három-négyszer többször fordul elő, mint a férfiaknál. A nemi különbségek mechanizmusai a reumás ízületi gyulladásban nem tisztázottak. Az interleukin-1 és a TNF szerepet játszik az RA patogenezisében. A legújabb munka kimutatta, hogy a 17β-ösztradiol (E2) IL-1α mRNS expressziót indukált a reumás fibroblaszt-szerű sejtvonalban, valamint RA-betegek primer szinoviális sejtjeiben. 52 Az IL-1α E2 általi indukciója ERα-függő volt, és a corepresszor, a hiszton-dezacetiláz ERa-tól való disszociációjának eredménye. Ez az SP1 transzkripciós aktivitás növekedését eredményezte az IL-1α gén promoterén belül a GC-ben gazdag régión keresztül. 52
Cutolo és munkatársai munkája rávilágított az ösztrogén szerepére a rheumatoid arthritisben. 38 Azt javasolták, hogy az ösztrogének szabályozzák a humorális immunitást, míg az androgének és a progeszteron ugyanazt a választ csökkentik. Jelezték, hogy az immunrendszer ösztrogén-szabályozásában számos tényező játszik szerepet, beleértve az androgén/ösztrogén arányt, a nemi hormonok cirkadiánszintjét, a gyulladásos citokinek, például a TNF-α, az IL1, az IL6 fokozott aromatáz aktivitását és a 17β- ösztradiol. A szerzők azt feltételezték, hogy a férfi reumás ízületi gyulladásban szenvedő betegek jobb válasza az anti-TNF terápiára ennek a hormonális szintnek köszönhető az ízületi folyadékban. 38
Sjögreni szindróma (SS)
A nőknél a Sjögren-szindróma 13-szor gyakoribb, mint az SS-vel küzdő férfiaknál. Az ösztradiol rendellenes hidroxilezésével rendelkező aromatázhiányos egerekben spontán kialakul egy limfoproliferatív autoimmun betegség, amely hasonlít a Sjögren-szindrómára. 53 Az ösztrogénhiány autoimmun exocrinopathiát eredményezhet, amely egészséges egerekben hasonlít a Sjögren-szindrómára. 54 Egészséges C57 BL/6 egerek petefészek eltávolítása az apoptotikus hámsejtek szignifikáns növekedését eredményezte a nyálmirigy sejtjeiben, ami a fokozott α-fodrin hasítással járt együtt. Ez utóbbi fontos autoantigén a Sjögren-szindrómában. Az in vivo munka kiterjesztése in vitro vizsgálatokra tamoxifennel kezelt donorok tenyésztett egér- vagy humán nyálmirigy-sejtjeivel 120 Kd α-fodrin hasítási termékének bizonyítékát mutatta. Sőt, az α-fodrin-reaktív T-sejtek petefészek-eltávolított, súlyos kombinált immunhiányos egerekbe történő átvitelével a Sjögren-szindrómához hasonló autoimmun exocrinopathiában részesültek alakultak ki. 54 Ez azt jelzi, hogy az ösztrogénhiány befolyásolhatja az autoantigén hasítását, és autoimmun exocrinopathiát eredményezhet a posztmenopauzás nőknél. 54.
Neurológiai betegségek
Az autoimmunitás nemi különbségeit alaposan tanulmányozták kísérleti allergiás encephalomyelitisben (EAE), a sclerosis multiplex modelljében, amelyben a nők hajlamosabbak a betegség kialakulására. Az EAE-ban végzett munka fókusza az immunrendszer összes paraméterét felölelte: sejtes, humorális, citokinek, kemokinek és gének. Citokineket és számos proinflammatorikus mediátort vizsgáltak. Az egyik legutóbbi citokin, az IL-13, amelyet az aktivált T-sejtek termelnek, számos hatással bír, beleértve a gyulladásos citokinek termelésének gátlását, az MHC II. Osztályú expresszió monocitákon történő szabályozását, anti-CD40-függő IgG/IgE osztályú kapcsoló indukcióját és IgG, IgM szintézis B sejtekkel. 55 A legújabb munkák azt mutatták, hogy a nőknél az EAE-érzékenység különbségét befolyásolják az IL-13 nemspecifikus proinflammatorikus hatásai, amelyek részben a Th1-indukáló citokinek és az MHC II vagy CD11b + makrofágok uregegulációján keresztül valósulnak meg. Úgy tűnik, a hatékony autoimmun válasz kiváltása érdekében stabil kapcsolatnak kell lennie a CD4 + T-sejtek és a dendritikus sejtek között. Ez utóbbi kapcsolatot a T-szabályozó sejtek gátolhatják. 57
A myasthenia gravisban (MG), amely egy neurológiai humán autoimmun betegség klasszikus klinikai modellje, korábban beszámoltunk az MG-vel rendelkező nők thymusjában a megváltozott sejtpopulációról. 58 A legfrissebb jelentések az ERα fokozott expresszióját jelezték timocitákon, és mind az ERα, mind az ERβ szintjét megnövelték az MG betegek perifériás vér mononukleáris sejtjeinek T-sejtjein. 59 A megnövekedett ösztrogénreceptor-expresszió MG-ben kifejezett volt a CD4 + alcsoportokon, és feltételezhető, hogy a proinflammatorikus citokinek feleslegének köszönhető. 59
- Body Constitution - áttekintés a ScienceDirect témákról
- Testsúlycsökkenés - áttekintés a ScienceDirect témákról
- Boletus edulis - áttekintés a ScienceDirect témákról
- Alapanyagcsere - áttekintés a ScienceDirect témákról
- Agysúly - áttekintés a ScienceDirect témákról