A „Calea zacatechichi” álomfű, nefrotoxicitás értékelése emberi vese proximális tubulussejtek alkalmazásával
Miriam E. Mossoba
Élelmiszerbiztonsági és Alkalmazott Táplálkozási Központ (CFSAN), Alkalmazott Kutatási és Biztonsági Értékelési Iroda (OARSA), Toxikológiai Osztály (DOT), Amerikai Élelmiszer- és Gyógyszerügyi Hivatal (US FDA), Neurotoxikológiai és In vitro toxikológiai részleg (NIVTB), 8301 Muirkirk Road, Laurel, MD 20708, USA
Thomas J. Flynn
Élelmiszerbiztonsági és Alkalmazott Táplálkozási Központ (CFSAN), Alkalmazott Kutatási és Biztonsági Értékelési Iroda (OARSA), Toxikológiai Osztály (DOT), Amerikai Élelmiszer- és Gyógyszerügyi Hivatal (US FDA), Neurotoxikológiai és In vitro toxikológiai részleg (NIVTB), 8301 Muirkirk Road, Laurel, MD 20708, USA
Sanah Vohra
Élelmiszer-biztonsági és Alkalmazott Táplálkozási Központ (CFSAN), Alkalmazott Kutatási és Biztonsági Értékelési Iroda (OARSA), Toxikológiai Osztály (DOT), Amerikai Élelmiszer- és Gyógyszerügyi Hivatal (US FDA), Neurotoxikológiai és In vitro Toxikológiai Osztály (NIVTB), 8301 Muirkirk Road, Laurel, MD 20708, USA
Paddy Wiesenfeld
Élelmiszerbiztonsági és Alkalmazott Táplálkozási Központ (CFSAN), Alkalmazott Kutatási és Biztonsági Értékelési Iroda (OARSA), Toxikológiai Osztály (DOT), Amerikai Élelmiszer- és Gyógyszerügyi Hivatal (US FDA), Neurotoxikológiai és In vitro toxikológiai részleg (NIVTB), 8301 Muirkirk Road, Laurel, MD 20708, USA
Robert L. Sprando
Élelmiszer-biztonsági és Alkalmazott Táplálkozási Központ (CFSAN), Alkalmazott Kutatási és Biztonsági Értékelési Iroda (OARSA), Toxikológiai Osztály (DOT), Amerikai Élelmiszer- és Gyógyszerügyi Hivatal (US FDA), Neurotoxikológiai és In vitro Toxikológiai Osztály (NIVTB), 8301 Muirkirk Road, Laurel, MD 20708, USA
Absztrakt
Az étrend-kiegészítők, köztük a gyógynövényes gyógyszerek használatának közelmúltbeli növekedése szükségessé teszi a biztonsági profiljuk vizsgálatát. Az „álomgyógynövényt”, a Calea zacatechichi-t már régóta használják a hagyományos népi gyógyászatban különböző célokra, és jelenleg az Egyesült Államokban forgalmazzák gyógyászati célokra, beleértve a cukorbetegség kezelését. Annak ellenére, hogy a veserendszer a xenobiotikus toxicitással szemben eredendően sérülékeny, nem állnak rendelkezésre biztonsági vizsgálatok a gyógynövény nefrotoxikus potenciáljáról. Ezenkívül a cukorbetegséggel társult vesebetegségek magas gyakorisága miatt különösen fontos a C. zacatechichi biztonsági szűrése. Az emberi proximális tubulus HK-2 sejteket ennek a gyógynövénynek növekvő dózisainak tettük ki az ismert toxikus és protektív kontroll vegyületek mellett, hogy megvizsgáljuk a C. zacatechichi lehetséges toxicitási hatásait a kontroll vegyületekhez viszonyítva. Értékeltük mind a celluláris, mind a mitokondriális funkcionális változásokat, amelyek összefüggésben álltak az étrend-kiegészítő toxicitásával, és megállapítottuk, hogy még alacsony dózisok esetén is szignifikáns volt a celluláris toxicitás bizonyítéka. Ezen túlmenően ezek a megállapítások korrelálnak a nephrotoxicitás biomarkerek jelentősen megemelkedett szintjével, ami további támogatást nyújt e növényi étrend-kiegészítő biztonságosságának további vizsgálatához.
1. Bemutatkozás
A Calea zacatechichi (más néven Calea ternifolia vagy „Álomgyógynövény”) Közép-Amerikában őshonos virágos növény, és nagy hagyománya van az őshonos kultúrák gyógynövényként való alkalmazásának [1]. A belélegzéssel (dohányzás) vagy a lenyeléssel (mint tea) történő expozíciót elsősorban a világos álom ideiglenes fokozására használják. Széles körben használják emésztőrendszeri és endokrin rendszerrel kapcsolatos problémák kezelésére is [2]. Nemrégiben étrend-kiegészítőként került forgalomba a cukorbetegség kezelésében, mivel hipoglikémiás hatásokat képes kiváltani [3–5], bár hatásmechanizmusa (i) továbbra sem tisztázott.
A C. zacatechichi oneirogén és egyéb biológiai hatásait részben a flavonjaiknak és a germakrolid komponenseiknek tulajdonítják [6–10]. A flavonok azonban a flavonoidok egy csoportját képviselik, amelyekről kimutatták, hogy citotoxikus hatásokat hordoznak részben a citokróm P450 enzim expressziójának indukciója révén [11–13]. Ezenkívül a csíra-makrolidok a szeszkviterpén-laktonok osztályába tartoznak, amelyek szintén negatív hatással lehetnek mind a prokarióta, mind az emlős sejtekre [14]. Mind a flavonoidok, mind a szeszkviterpén-laktonok citotoxicitását rák elleni terápiában alkalmazták [15, 16].
2. Anyagok és módszerek
2.1. A Calea zacatechichi kivonat jellemzése
A Mississippi Egyetemen, a Nemzeti Természeti Kutatási Központban (NCNPR) letétbe helyezett C. zacatechichi utalványmintákat (NCNPR # 2443) hitelesítették makroszkópos és mikroszkópos módszerekkel egy NCNPR botanikus. Az NCNPR liofilizált formában C. zacatechichi metanolos kivonatot biztosított, amelyet sötétben, 4 ° C-on vákuumkamrában tároltunk. A C. zacatechichi szárított kivonatát LC/QTof módszerrel elemeztük a korábban leírtak szerint [29]. A vegyületeket feltételezhetően azonosítottuk az analiták pontos tömegének és az irodalomban közölt C. zacatechichi komponenseknek [8, 30–33].
2.2. Sejtkultúra és kezelések
A HK-2 sejteket növesztettük, fenntartottuk és a korábban leírtakhoz hasonló módon kezeltük [29]. A C. zacatechichi, a nephrotoxicant (pozitív kontroll) cisz-diamineplatinum (II) diklorid (cisplatin) (Sigma-Aldrich, St. Louis, MO) és a nephroprotectív (negatív kontroll) valproinsav (Sigma-Aldrich) törzsoldatát készítettük. poruk lemérésével, DMSO-ban történő feloldásával és ezt a keveréket tápközeggel hígítva 0,4% vagy kevesebb végső DMSO törzsoldatra. A sejteket egy éjszakán át inkubáltuk, és háromszor ismételtük 24 órán át a 0–1000 μg/ml dózistartományban.
2.3. Citotoxicitási vizsgálat
A kezeléssel kapcsolatos citotoxicitást a bevett CellTiter-Glo sejt-életképességi vizsgálattal (Promega, Madison, WI) határoztuk meg, a gyártó ajánlásait követve. Ennek a lumineszcens vizsgálatnak az az előfeltétele, hogy az ATP termelése közvetlenül arányos legyen a sejt életképességével, mivel az ATP központi szerepet játszik a létfontosságú sejtes folyamatokhoz szükséges energiában. A fekete falú, tiszta alsó 96 lyukú lemezeken kezelt sejteket 30 percig szobahőmérsékletre egyensúlyoztuk, és ezalatt a külső üregekben lévő vizet körülbelül 100 ul kezelési vagy csak táptalaj kontrollokkal helyettesítettük. Ezt követően minden térbe azonos térfogatú CellTiter-Glo munkaoldatot adtak. A lemezeket 2 percre egy orbitális rázógépre helyeztük a sejtek lízisének előidézése érdekében, majd további 10 percig inkubáltuk, mielőtt az OMG Fluorostar lemezolvasón (BMG LABTECH, Ortenberg, Németország) leolvastuk az egyes üregekből kibocsátott lumineszcencia szintjét.
2.4. Reaktív oxigénfaj vizsgálata
A reaktív oxigénfajok (ROS) mennyiségi meghatározását Promega ROS-Glo H2O2 lumineszcencia-alapú detektáló rendszerével határoztuk meg, és az adatokat normalizáltuk a sejtek életképességéhez. 24 órás közvetlen C. zacatechichi expozíció után a sejteket H2O2 szubsztráttal és detektáló reagenssel inkubáltuk, a gyártó utasításainak megfelelően. A lumineszcenciát egy OMG Fluorostar lemezolvasón olvastuk le.
2.5. Mitokondriális membrán potenciálvizsgálat
A mitokondriális membránpotenciál (MMP) változását a JC-10 ratiometrikus festékkel értékeltük (Enzo, Farmingdale, NY). A közvetlenül a C. zacatechichi-nek kitett HK-2 sejteket 20 uM JC-10-vel (végső koncentráció) 2 órán át festettük, mostuk, majd lemezolvasóval (OMG Fluorostar) leolvastuk. A gerjesztést 485 nm-en állítottuk be, és az emissziót 520 és 590 nm-en mértük. Megállapítottuk azt is, hogy a kivonat vagy a közeg önmagában nem eredményezett jelentős kibocsátási jeleket.
2.6. Nefrotoxicitási biomarker vizsgálatok
A vesék toxicitásának biomarkereinek szintjét 24 órán át C. zacatechichivel, ciszplatinnal és valproinsavval 333 és 111 μg/ml dózisban kezelt sejtek tenyészetei felülúszók értékelték: veseméret-1 (KIM-1), albumin, cystatin C és béta-2-mikroglobulin (B2M) segítségével humán vesetoxicitási készleteket (Bio-Rad, Hercules, CA). A gyártó eljárása szerint a lemezeket blokkoltuk, mostuk és inkubáltuk mintákkal, standard oldat detektáló antitestekkel, mielőtt végső mosást kaptunk volna. A lemezeket Luminex 200 készülékkel (Bio-Rad) olvastuk. A biomarker expressziós szinteket normalizáltuk a sejtek életképességéhez.
2.7. Statisztika
A Microsoft Excel és a Prism (GraphPad, San Diego, Kalifornia) felhasználásával számolták és elemezték az összes összegyűjtött adatot. A diákok t-tesztjeit vagy kétutas ANOVA-kat használtak annak meghatározására, hogy a dózishoz illesztett kezelési hatások statisztikailag szignifikánsak-e 0,01 vagy 0,001 alatti P-értékeken, amint azt jelezték.
3. Eredmények
3.1. A Calea zacatechichi kivonat jellemzése
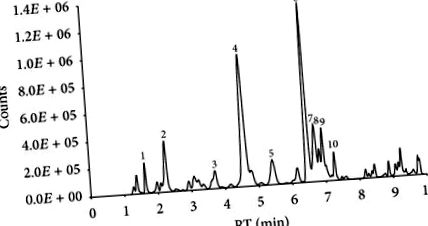
LC-nagy felbontású MS 231 teljes molekuláris tulajdonságot talált a C. zacatechichi kivonatban. Ezek közül 24 tulajdonság pontos tömege megegyezik a C. zacatechichi jelentett komponenseinek tömegével (1. ábra). A csúcstérfogaton alapuló fő komponensek, a calein A, a ciliarin, az acacetin és a kalealakton C az ismert vegyületek körülbelül 50% -át és az összes vegyület 8% -át tették ki [8, 30–33].
A C. zacatechichi kivonat LC nagy felbontású tömegspektroszkópiával végzett kémiai jellemzéséből kivont teljes vegyület-kromatogram. A feltételezett vegyület azonosítást a pontos tömeg és a C. zacatechichi ismert komponenseinek tömegével való összehangolásával végeztük [8, 30–33]. (1) Ciliarin, (2) zexbrevin, (3) szeszkviterpén-lakton, (4) D-kalein, (5) 1-β-acetoxi-acatechinolid, (6) Calein A, (7) 1-oxo-zacatechinolid, (8) kalealakton E, (9) kalealakton és (10) acetoxikalekulatolid.
3.2. A C. zacatechichi erősen gátolja a HK-2 sejtek életképességét
A C. zacatechichi nephrotoxicitásának vizsgálatához ATP-alapú sejtek életképességi vizsgálatot végeztünk HK-2 sejteken, amelyeket 6 dózisú 0 és 1000 μg/ml közötti koncentrációval kezeltünk 24 órán át. Összehasonlításképpen, a sejteket 24 órán át kezeltük az ismert nefrotoxikus vegyület, a ciszplatin és az ismert nefroprotektáns, valproinsav dózisnak megfelelő koncentrációival is. Megállapítottuk, hogy a ciszplatin a sejt életképességének jelentős csökkenését indukálta a
12 μg/ml tesztelt dózis (P 2. ábra). Hasonlóképpen, a C. zacatechichi szignifikáns citotoxicitását 37,0 μg/ml-től kezdve detektáltuk (P 2. ábra. A nephroprotektortól elvárható, hogy a valproinsav számított LC50-értéke 3866 μg/ml-nél meglehetősen magas, mivel sejtje fennsíkjának alakja életképességi görbe.
- Álomgyógynövény Calea Zacatechichi (Az istenek gyógynövényei) 50 gramm
- A súlyvesztés időbeli értékelése krónikus vesebetegségben szenvedő macskáknál
- Clenbuterol (Clen) - 5 dolog, amit szeretnél tudni, mielőtt használnád
- A vesebetegség elleni küzdelem jobb étrenddel, fogyással és dohányzásról való leszokással - Harvard Health
- Étkezés az álomban - mit jelent Frissítve ▷